Концентрация - компонент - система
Cтраница 2
 |
Определение чувствительности конкурентных методов. анализа. [16] |
Рассмотрим на ряде конкретных примеров, как зависит чувствительность анализа от концентраций компонентов системы и констант связывания. [17]
Возникающий при этом градиент химического потенциала, который зависит от вида и концентрации компонентов системы, вызывает перемещение веществ в пористой среде, т.е. градиент химического потенциала становится движущей силой процесса взаимодействия системы. В большинстве технологических операций, основанных на применении химпродуктов, указанный процесс носит диффузионный характер. Вследствие этого движение пластовой воды, представляющей коллоидный раствор, сопровождается различными видами взаимодействия с твердыми частицами породы. При заводнении пластов с применением пресных вод диффузионный переход частиц пород в раствор сопровождается увеличением коэффициента проницаемости пласта. [18]
Как зонная плавка, так и фракционная кристаллизация основаны на том, что концентрации компонентов системы в твердой и жидкой фазах различны. Основное различие между зонной плавкой и фракционной кристаллизацией состоит в том, что в первом случае одновременно плавится только часть материала, а не весь материал. Такая особенность в ведении процесса в огромной степени повышает эффективность кристаллизации как способа разделения и открывает новые пути ее применения. [19]
Фазовое состояние системы определяется внешним энергетическим воздействием ( температура, давление) и концентрацией компонентов системы в фазах. Эти превращения происходят с изменением энергии связи между частицами, поэтому процессы фазовых переходов сопровождаются поглощением или выделением тепловой энергии, которая называется скрытой теплотой превращения. Рассмотрим это на примере железа. Напомним, что более устойчиво состояние системы с наименьшим значением термодинамического потенциала. [20]
Пространственно-временные диссипативные структуры типа бегущей волны возникают в связи с образованием предельного цикла, когда концентрации компонентов системы не только колеблются во времени, но и одновременно изменяют свои координаты в пространстве. Такая система допускает волнообразное движение, при котором локальные колебания не организуются для образования стоячей волны, а принимают участие в общем продвижении волновых фронтов. Диссипативная структура в этом случае реализуется по типу бегущей волны во времени и пространстве. Система может обладать несколькими стационарными состояниями, которые соответствуют одному и тому же значению параметра. Если, например, а а0, то а, с - устойчивы, a b - неустойчивое состояние. Тогда части кривой АВ и DC представляют собой ветви устойчивых, а ЕС - ветвь неустойчивых стационарных состояний. При достижении бифуркационных значений параметра ( а, а) происходят скачкообразные переходы С А и BD в экстремальных точках В и С кривой / ( А, а) 0 так что неустойчивые состояния на участке ВС практически никогда не реализуются в действительности. Таким образом, реализуется замкнутый гис-терезисный цикл ABDCA, в котором в результате изменения параметра система проходит ряд стационарных состояний, отличающихся друг от друга при одних и тех же значениях а в зависимости от направления движения. Системы, обладающие способностью функционировать в одном из двух устойчивых стационарных состояний, принято называть триггерными. [21]
Эта система имеет одну степень свободы, поэтому до известного предела можно изменять температуру или концентрацию компонентов системы без нарушения равновесия системы. [22]
Численное значение AG зависит от того, какую константу равновесия мы используем: Кр, которая относится к давлениям компонентов системы, или Кс, которая относится к концентрациям компонентов системы. Что же касается знака изменения стандартной свободной энергии, то он не должен зависеть от того, какую из констант равновесия мы используем. Для химических реакций, в которых участвуют газы, величины Кс и КР будут равны друг другу, если число молей газообразных реагентов равно числу молей газообразных продуктов. [23]
А, В, С и D, что обусловливает изменение свойств системы. В каждый момент титрования концентрации компонентов системы определяются константой равновесия реакции и количеством добавленного титранта. По мере накопления количественных изменений происходит качественное изменение свойств системы. [24]
Диаграммы состояния системы позволяют определить влияние физико-химических факторов на состояние системы. Изменяя температуру, давление, концентрацию компонентов системы, можно сместить равновесие, перевести систему из одного равновесного состояния в другое и довести реакцию до конца. Допустимое одновременно число фаз в системе изменяется в зависимости от ряда факторов. [25]
 |
Кинетические кривые НИИ схемы - в условиях Qa Lia I - aa ( CM. ГЛЗВу 10. [26] |
Приведем полученные таким образом выражения для концентраций компонентов системы (11.1) - ( П-2) в различных условиях проведения процесса. [27]
Константа равновесия процесса определяется энергиями связи L - - M - - и L - - Mj. Равновесие может быть смещено изменением условий проведения реакции, в частности концентрации компонентов системы. Если энергия связи L - - Mi значительно больше энергии связи L - - M -, то обмена по приведенной схеме практически не происходит. [28]
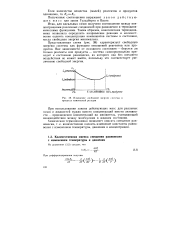 |
Изменение свободной энергии системы в процессе химической реакции. [29] |
Итак, для идеальных газов получено соотношение между концентрациями различных соединении при равновесии и термодинамическими функциями. Таким образом, классическая термодинамика позволила определить направление реакции и количественно оценить концентрации компонентов системы в состоянии, когда свободная энергия минимальна. [30]
Страницы: 1 2 3 4