Концентрация - компонент - реакционная смесь
Cтраница 2
R - газовая постоянная; Т - абсолютная температура; / ( С) - функция концентраций компонентов реакционной смеси. [16]
Так как скорость реакции является функцией не только химической активности катализатора, но и режимных параметров процесса ( температуры Т, концентрации компонентов реакционной смеси С и общего давления Р), активность каталиаа-тора - понятие конкретное, связанное с условиями проведения реакции и со степенью ее завершенности. [17]
При заданных внешних условиях ( температура, давление, среда, в которой происходит процесс) скорость химического превращения является функцией только концентраций компонентов реакционной смеси. Уравнение, описывающее зависимость скорости химического процесса от концентрации компонентов реакционной смеси, называется кинетическим уравнением химического процесса. [18]
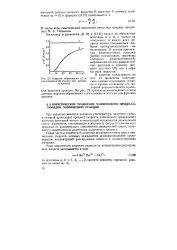 |
Скорости образования ( 1 и расходования ( 2 этилена при крекинге пропана. [19] |
При заданных внешних условиях ( температура, давление, среда, в которой происходит процесс) скорость химического превращения является функцией только концентраций компонентов реакционной смеси. Уравнение, описывающее зависимость скорости химического процесса от концентрации компонентов реакционной смеси, называется кинетическим уравнением химического процесса. [20]
Данные всех опытов были пересчитаны и представлены в виде полей точек для каждой из зависимых переменных, которыми являлись температура слоя катализатора и концентрации компонентов реакционной смеси. Значения зависимых переменных были нанесены на плоскость в системе координат: время контакта - зависимая переменная. Задача расшифровки кинетики заключалась в подборе такой системы дифференциальных уравнений материального и теплового баланса, которая бы максимально удовлетворяла экспериментальным результатам. [21]
Входящая в правые части уравнений (6.1) и (6.2) величина р - ( с, Т) представляет собой скорость химической реакции как функцию вектора концентраций компонентов реакционной смеси и температуры. Вид функциональной зависимости устанавливается экспериментально с учетом соображений, изложенных в гл. [22]
На основе гипотезы об элементарных реакциях, протекающих на поверхности катализатора, и об энергетических свойствах поверхности катализатора ( энергетически однородная, неоднородная и характер неоднородности) с помощью этой теории можно построить кинетическую модель, включающую в общем случае систему стехиометрических уравнений ( базис стехиометрических уравнений) и уравнения, определяющие скорости изменения концентраций компонентов реакционной смеси в зависимости от температуры и состава реакционной смеси. [23]
Такой режим называют стационарным режимом или стационарным состоянием. В закрытой системе концентрации компонентов реакционной смеси изменяются за счет протекания реакций, что ведет за собой изменения скоростей реакций. Следовательно, в закрытых системах химические реакции протекают нестационарно. [24]
При заданных внешних условиях ( температура, давление, среда, в которой происходит процесс) скорость химического превращения является функцией только концентраций компонентов реакционной смеси. Уравнение, описывающее зависимость скорости химического процесса от концентрации компонентов реакционной смеси, называется кинетическим уравнением химического процесса. [25]
 |
Схематическое представление зависимости выходных переменных х ( от входных переменных и и t ] j. [26] |
Так, скорость подачи газа ограничена мощностью компрессоров, температура смеси на входе в реактор - возможностями теплообменников. По соображениям взрывобезопасности, соответствующие ограничения могут налагаться на концентрации компонентов реакционной смеси. [27]
Будем считать, что процессы конвекции и принудительного перемешивания отсутствуют, а концентрации компонентов реакционной смеси в газовой фазе постоянны. Будем также полагать, что реакция может протекать на поверхности, раздела фаз или в объеме жидкости. [28]
Будем считать, что процессы конвекции и принудительного перемещения отсутствуют, а концентрации компонентов реакционной смеси в газовой фазе постоянны. Примем, что реакция может протекать на поверхности раздела фаз. Возможны стадии этого процесса: диффузия газа к поверхности раздела фаз, его адсорбция на поверхности раздела фаз, растворение адсорбированного газа в жидкости. Очевидно, что при наличии газообразного продукта реакции указанная последовательность стадий реализуется и в обратном направлении. Приведенное разделение стадий в известной мере условно, поскольку, например, адсорбция и особенно растворение могут одновременно являться и актом химической реакции. [29]
Таким образом, при изменении соотношения реагирующих веществ значение AG меняется от - оо до оо. Очевидно, что сравнивать химическое сродство двух или нескольких реакций, не оговорив предварительно концентрации компонентов реакционной смеси, невозможно. С целью возможности сравнения ДО различных реакций, а также для последующих расчетов констант равновесия введена величина AG, называемая стандартным химическим сродством. [30]
Страницы: 1 2 3