Концентрация - компонент - реакционная смесь
Cтраница 3
Эти методы основаны на реализации в лабораторном реакторе режима идеального смешения. Часто такие реакторы называют безградиентными, однако это определение неточно - если в слое катализатора совсем нет градиентов концентраций компонентов реакционной смеси, то нет и химических превращений. [31]
На самом деле эта неадекватность только кажущаяся. При заданных внешних условиях ( температура, давление, среда, в которой проходит процесс) скорость реакции является функцией только концентраций компонентов реакционной смеси. Та же зависимость получается и при определении скорости из стационарной концентрации компонента в реакторе идеального смешения. Определяемая по (11.14) величина соответствует определенному составу реакционной смеси в реакторе. [32]
Кинетическое уравнение химического процесса не зависит от того, проводится реакция в открытой или замкнутой системе. Однако в открытой системе производная от концентрации по времени уже не является скоростью реакции, а соотношения (11.10) не могут быть использованы для установления связи между концентрациями компонентов реакционной смеси. Последнее, конечно, не означает, что концентрации компонентов реакционной смеси не зависят друг от друга. [33]
Ур Урект, VpeKT / Vp составляет большую конечную величину. Тогда при некотором конечном времени пребывания реагентов в системе ( некоторой конечной интенсивности обмена системы с окружающей средой), в соответствии с исходными условиями, за счет химической реакции установится некоторая постоянная величина конверсии реагентов и соответствующие ей концентрации компонентов реакционной смеси. [34]
 |
Схема различных возможностей столкновений. ( Число возможных столкновений определяется произведением числа молекул А на число молекул В в заданном объеме. [35] |
С помощью теории столкновений рассмотрение простейшей реакции между гипотетическими молекулами А и В можно распространить на реальные химические реакции, в которых одновременно принимает участие большое число молекул. Но вместо того чтобы пользоваться данными об истинном числе молекул в единице объема, теория столкновений прибегает к единицам измерения концентрации, которые были введены в гл. Таким образом, концентрации компонентов реакционной смеси могут быть выражены в молях на литр ( молярность) или представлены парциальными давлениями. Для обозначения концентраций реагентов или продуктов реакции принято использовать квадратные скобки: например, [ А ] означает число молей вещества А в 1 л раствора. Если вещество А представляет собой газ, для указания его концентрации обычно используется символ РА, означающий парциальное давление газа А. [36]
Если скорость этого воздействия невелика и за время проведения каталитического процесса не происходит заметного изменения состава катализатора, то удельная каталитическая активность зависит от предшествующей обработки катализатора. Если же стационарный состав катализатора достигается быстро, то его изменение в результате воздействия реакционной смеси оказывает существенное влияние на кинетику каталитической реакции. Зависимость скорости реакции от концентрации компонентов реакционной смеси определяется, следовательно, не только изменением числа столкновений реагирующих частиц, участвующих в лимитирующей стадии реакции, но и изменением константы скорости реакции вследствие воздействия реакционной смеси на состав и свойства катализатора. Борескова на значение этого фактора в катализе получили за последние годы подтверждение и развитие в работах ряда советских и зарубежных ученых. [37]
Кинетическое уравнение имеет две важные особенности, отличающие его от уравнений кинетических кривых для компонентов реакции. Во-первых, вид кинетического уравнения ке зависит от того, протекает процесс в замкнутой или открытой системе. Поэтому зависимости скорости реакции от концентраций компонентов реакционной смеси и значения кинетических параметров, входящих в эти зависимости, установленные в экспериментах, проведенных в открытой системе, могут непосредственно использоваться для обработки и трактовки данных, получаемых для той же реакции в замкнутой системе. Это весьма существенно, поскольку, как уже указывалось, скорость реакции в открытой системе может, как правило, быть измерена со значительно большей точностью, чем в замкнутой системе. [38]
Кинетическое уравнение химического процесса не зависит от того, проводится реакция в открытой или замкнутой системе. Однако в открытой системе производная от концентрации по времени уже не является скоростью реакции, а соотношения (11.10) не могут быть использованы для установления связи между концентрациями компонентов реакционной смеси. Последнее, конечно, не означает, что концентрации компонентов реакционной смеси не зависят друг от друга. [39]
Гетерогенные реакции обычно локализуются в некоторых областях реакционного пространства. В связи с этим в реакционном пространстве возникают градиенты концентраций и температуры и, соответственно, потоки вещества и тепла. Количественная характеристика этих процессов чрезвычайно существенна, так как наряду с химической реакцией именно они определяют концентрации компонентов реакционной смеси и температуру в реакционной зоне. [40]
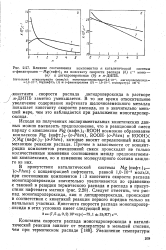 |
Влияние соотношения компонентов п каталитической системы. [41] |
КООН возможно образование комплексов Mg ( нафт. Причем в зависимости от концентрации компонентов реакционной смеси происходят не только количественные изменения соотношения между предполагаемыми комплексами, но и изменение молекулярного состава каждого из них. [42]
Страницы: 1 2 3