Концентрация - металл
Cтраница 4
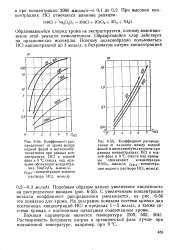
Увеличение концентрации металла в растворе способствует повышению скорости катодного процесса. Однако такая закономерность наблюдается только до определенного предела, после которого происходит увеличение поляризации с повышением концентрации электролита. Опыты показали, что самая малая катодная поляризация наблюдается в электролите, содержащем 0 075 молъ / л комплексной соли палладия и 0 15 молъ / л хлористого аммония. [46]
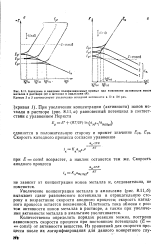 |
Катодные и анодные поляризационные кривые при изменении активности попав. [47] |
Увеличение концентрации металла в амальгаме ( рис. 8.11 6) вызывает сдвиг равновесного потенциала в отрицательную сто рону и возрастание скорости анодного процесса; скорость катодного процесса остается неизменной. Плотность тока обмена с ростом активности ионов металла в растворе, а также при увеличении активности металла в амальгаме увеличивается. [48]
Уменьшение концентрации металлов вдвое по отношению к концентрации окислов Грифит объяснил тем, что промотор действует своими валентными силами, и если окисел оказывает влияние на один активный центр катализатора, то металл - на два активных центра. [49]
Примем концентрацию металла в натеках электролита за 100 тыс. часть / млн. После промывки концентрация должна снизиться до 10 часть / млн. Объем натеков составляет один литр в час. [50]
Благодаря этому концентрация металла М значительно понизится, а концентрация свободного лиганда остается столь низкой, что он уже ее будет мешать. [51]
СА - концентрация металла на поверхности и с4 - его концентрация в центре капли. [52]
С - концентрация металла в растворе; / - толщина светопоглощающего слоя, см. При сопоставлении данных метода Комаря и метода с учетом поглощения избытка красителя видно, что найденные обоими методами коэффициенты близки между собой по абсолютной величине. [53]
Так как концентрация металлов в фазе ТБФ значительно превышает концентрацию кремнефтористоводородной кислоты, для расчета степени образования комплексов урана, нептуния, плутония и циркония необходимо было определить значения равновесной концентрации [ НА ] для различных значений общей концентрации H2SiFe и HNOg. [54]
Так как концентрация титруемых металлов в большинстве случаев составляет 10 - 4 - 10 - 2 М ( в среднем [ M ] t 10 - 3), ясно, что величина эффективной константы устойчивости образовавшегося хелатного комплекса должна быть равна по меньшей мере 107, если ошибка титрования не должна превышать 1 %, При титровании магния раствором ЭДТА эти условия хорошо соблюдаются при рН 10, тогда как титрование бария уже представляет собой предельный случай. При индикации точки эквивалентности с помощью инструментальных методов значение рМэ можно определить с большей точностью, следовательно, АрМ и ошибка титрования оказываются меньше. Однако при комплексо-нометрических титрованиях скачок рМ в конечной точке часто бывает настолько большим, что и визуальный метод дает очень точные результаты. В этом случае нет необходимости определять рМэ с большой точностью; более того, индикатор в точке эквивалентности резко переходит из одной формы в другую, окрашенную иначе. [55]
Результаты определения концентрации металлов в шариках гех же размеров, выбранных из общей массы циркулирующего равновесного катализатора, показали, что при работе катализатора возрастает концентрация имеющихся металлических примесей и дополнительно откладываются никель, ванадий и цинк. [56]
При повышении концентрации металла образуются кластеры из металлических ионов. При концентрациях выше 3 М растворы приобретают медный цвет с металлическим блеском. [57]
С увеличением концентрации металла коэффициент распределения уменьшается, на рис. 6 - 56 это показано для хрома. На диаграмме показана система кривых для постоянных концентраций НС1 в пределах 1 - 5 моль / л, а также система кривых с постоянным начальным содержанием хрома. [59]
С увеличением концентрации металла в пламени до 10 М эффект ослабления атомных линий [2] и молекулярных полос у катода в ряде случаев уменьшается или же совсем не проявляется. Поэтому при таких добавках смещение ионизационного равновесия металлов у катода под действием электрического поля должно отсутствовать. [60]
Страницы: 1 2 3 4 5