Концентрация - мочевина
Cтраница 3
Отбирают из каждой пробирки 2 мл фильтрата и определяют концентрацию мочевины. Для этого к фильтратам добавляют по 2 мл цветного реактива ( содержащего диацетилмонооксим, тиосемикарбазид и соли железа. Пробы перемешивают и ставят в кипящую водяную баню на 15 мин. [31]
В работе отмечено, что начало реакции существенно зависит от концентрации мочевины в растворе. Так, при 500 мг / дм3 начало реакции наблюдается через 30 мин; при 70 - 80 мг / дм3 - через 2 - 3 ч; при 50 мг / дм3 - практически не наблюдается. [32]
 |
Действие метилолмочевины на мочевину. Кинетическая роль мочевины. [33] |
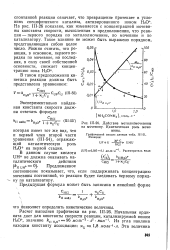
На рис. 111 - 26 показано, как изменяется с концентрацией мочевины константа скорости, вычисленная в предположении, что реакция - первого порядка по метилолмочевине, по мочевине и по катализатору. Такое влияние не может быть выражено порядком, представляющим собою целое число. [34]
Влияние солей на денатурацию белков иллюстрируется рис. 2, где показана концентрация мочевины, необходимая для того, чтобы вызвать денатурацию эдестина в присутствии различных солей. В более поздних исследованиях было установлено, что соли по эффективности располагаются совершенно аналогичным образо. [35]
Ионы аммония регистрируются ионоселективным электродом, причем величина аналитического сигнала пропорциональна концентрации мочевины. В качестве электрода для определения мочевины можно использовать покрытый уреазой СО2 - электрод, чувствительный к карбонат-ионам после их превращения в диоксид углерода. [36]
Пусть аи ( а - х) - начальная и текущая концентрации мочевины, b - концентрация спирта, си ( с х) - начальная и текущая концентрации аммиака. [37]
Ест - экстиикция стандартной пробы; 0 02 мг / мл - концентрация мочевины в стандартной пробе. [38]
Полученные результаты показали, что озонирование в течение 1 ч не снижает концентрации мочевины в растворе. [39]
Вследствие всасывания воды и растворенных в ней веществ в содержимом проксимального канальца растет концентрация мочевины, небольшие количества которой по концентрационному градиенту реабсорбируются в кровь. [40]
Расчет производят по формуле: С А / А2 16 65, где С - концентрация мочевины, ммоль / л; А1 - оптическая плотность опытной пробы; А2 - оптическая плотность стандартной пробы. [41]
Гидролиз мочевины в мягких условиях катализируется ферментом уреазой; ферментативный гидролиз применяют для аналитического определения концентрации мочевины. [42]
Время отклика электрода, чувствительного к мочевине, меняется от 60 до 180 с в зависимости от концентрации мочевины и толщины реакционного слоя. Стабильность электрода во времени достаточно хорошая, потенциометрическая активность и селективность остаются постоянными в течение более 5 месяцев. [43]
Потенциал, измеряемый электродом в растворе после гидролиза, определяется количеством иона аммония, а следовательно, концентрацией мочевины или уреазы. Кац и Кованс [27] изучали влияние различных ионов на реакции мочевины, катализируемые уреазой. В исследовании Гильбо и др. [23] сделана попытка определить фермент и субстрат одновременно. [44]
 |
Изменение плотности системы CO ( NH2 2 - NH3 - H2O при 15 С в зависимости от концентрации компонентов. [45] |
Страницы: 1 2 3 4 5