Концентрация - нитрат-ион
Cтраница 4
 |
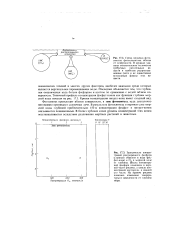
Распределение нитрата уранила.| Характерные участки кривых распределения ( у и х - концентрация нитрата уранила в органической и водной фазах. ( - дибутиловый эфир. 2 - диэтиловый эфир. 3 - ТБФ. [46] |
В качестве высаливающего агента нередко используют также азотную кислоту. Однако химизм действия азотной кислоты не сводится только к увеличению концентрации нитрат-иона и уменьшению активности воды. Как уже указывалось, при экстракции; из азотнокислых растворов актиноиды могут экстрагироваться и в форме оксониевых комплексных солей. Азотная кислота, особенно в присутствии других высаливателей, сама хорошо экстрагируется органическим растворителем. В растворе молекулы кислоты, так же как и молекулы нитрата уранила, сольва-тируются определенным количеством молекул растворителя. [47]
Элементы ( 1), которые в наиболее устойчивом валентном состоянии находятся в растворах в виде анионов кислот, извлекаются по реакциям анионного обмена, закономерности которых приведены в гл. Извлечение этих элементов, очевидно, должно снижаться при увеличении концентрации нитрат-ионов в водном растворе. [48]
Следует, однако, отметить, что в некоторых реакциях нитратные комплексы оказываются более способными к окислительно-восстановительной реакции, чем простые ионы. Скорость диспропорционирования U ( V), например, прямо пропорциональна концентрации нитрат-ионов. [49]
Эти элементы в нитратных системах могут быть отнесены к группе А, так как легко образуют нейтральные и анионные комплексы с нитрат-ионами. В соответствии с этим коэффициенты распределения указанных элементов в исследованных пределах концентраций нитрат-ионов в водной фазе ( 0 05 - 0 1 н) наиболее высоки при самой низкой концентрации этих ионов и снижаются по мере ее увеличения. [50]
 |
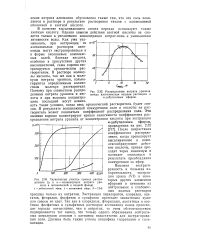
Бимолекулярные константы реакции между йодистым метилом и солями серебра. в - исходная концентрация водного раствора.| Влияние ионной силы на скорость реакции между AgN03 и СН31 при 25 С. [51] |
Если такой подход верен, то к2 должна линейно зависеть от произведения концентрации нитрат-ионов на квадрат среднего коэффициента активности. Значения коэффициента активности при 25 С известны [39], они приведены для некоторых значений концентрации в табл. 8.14. Помещенные там же рассчитанные значения к2 получены по уравнению к2 2 61 - Ю-3 - f - 1 72 - 10 1 [ NO3 ] у2 - Отсюда следует, что при концентрациях, превышающих 0 021 М, число молекул, реагирующих через тримо-лекулярный комплекс, становится больше, чем число молекул реагирующих по бимолекулярному механизму. Это возможно только в том случае, если энергия активации тримолекулярного процесса намного меньше, чем энергия активации бимолекулярной реакции. Снижение энергии активации при переходе к тримолекулярному механизму может быть связано с тем, что анион, приближаясь к метильному концу молекулы и не реагируя с ней химически, способствует электростатическому притяжению иона серебра, который приближается со стороны атома галогена на расстояние, соответствующее критическому расстоянию для атома иода. [52]
Анализируя уравнения ( 1.8 - 1.13), можно сделать вывод, что в зависимости от механизма экстракции коэффициент распределения Кр зависит от разных факторов. Действительно, при экстракции уранила нитрата ТБФ коэффициент распределения увеличивается с ростом концентрации нитрат-иона в водной фазе и ТБФ в органической фазе. Однако не следует забывать о довольно сложном изменении коэффициентов активности UO2 ( NO3) 2, ТБФ и разбавителя с изменением условий экстракции. При экстракции железа ( III) эфирами коэффициент его распределения растет с увеличением концентрации иона водорода, а при экстракции циркония р-дикетонами падает. [53]
 |
Влияние ионной силы на скорость реакции между AgNO3 и СН31 при 25 С.| Бимолекулярные константы реакции между йодистым метилом и солями серебра. в - исходная концентрация водного раствора. [54] |
Если такой подход верен, то kz должна линейно зависеть от произведения концентрации нитрат-ионов на квадрат среднего коэффициента активности. [55]
Полученная газовая смесь подается в по-глотительный сосуд с раствором, где происходит поглощение в результате гидролиза оксида азота ( V) с образованием нитрат-ионов. Измеряя ЭДС в растворе, определяют изменение потенциалов электродов, зависящее от изменения концентрации нитрат-ионов в растворе. [56]
Коэффициенты распределения продуктов деления и эффективность очистки от них урана и плутония регулируются концентрацией нитрат-иона в водной фазе и концентрацией свободного трибутилфосфата в органической фазе. В экстракционной колонне I в значительных концентрациях присутствуют два компонента - уранил нитрат и азотная кислота, - и они определяют концентрации нитрат-иона и свободного трибутилфосфата. [57]
Последнее объясняется тем, что глубинная океаническая вода богаче фосфором и азотом по сравнению с водой вблизи поверхности. Типичный профиль концентрации фосфат-ионов как функции глубины морской воды показан на рис. 17.3. Кривая концентрации нитрат-иона имеет сходный вид. Фотосинтез происходит вблизи поверхности, в зоне фотосинтеза, куда достаточно интенсивно проникают солнечные лучи. В результате фотосинтеза в верхнем слое морской воды глубиной приблизительно 150м концентрации фосфат - и нитрат-ионов оказываются пониженными. В более глубоких слоях уровень концентраций этих ионов восстанавливается вследствие разложения мертвых растений и животных. [59]
В ИЯЭ АН БССР разработана методика изучения кинетики жидкофазного нитрования окислов металлов, которые являются соответствующими аналогами осколков деления. Количество окисла, подвергшегося при данных условиях процессу нитрования, находится после соответствующей обработки пробы по концентрации нитрат-ионов в водной фазе. [60]
Страницы: 1 2 3 4 5