Концентрация - окислитель
Cтраница 1
Концентрации окислителя и восстановителя, указанные в табл. 1, сохранялись во всех опытах. [1]
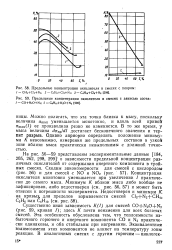 |
Предельные концентрации окислителя в смесях с хлором.| Предельные концентрации окислителя в смесях с закисью азота. [2] |
Концентрация окислителя монотонно уменьшается при увеличении / практически до самого мыса. Минимум К вблизи мыса либо вообще не зафиксирован, либо недостоверен ( см. рис. 56, 57) и может быть отнесен к погрешности эксперимента. [3]
Кроме концентрации окислителя и восстановителя, на величину окислительно-восстановительного потенциала влияет концентрация ионов водорода. [4]
Определяет концентрации окислителей и восстановителей, органических кислот и оснований. [5]
Кроме концентрации окислителя и восстановителя на величину окислительно-восстановительного потенциала оказывает влияние концентрация ионов водорода. Так, например, с увеличением концентрации ионов Н окислительно-восстановительный потенциал таких пар, у которых окисленная форма содержит кислород ( MnO4 -, CrO42 -, Cr2O72 -, AsO43 -), возрастает, а с уменьшением концентрации ионов Н падает. [6]
Кроме концентрации окислителя и восстановителя на величину окислительно-восстановительного потенциала оказывает влияние концентрация ионов водорода. Так, например, с увеличением концентрации ионов Н окислительно-восстановительный потенциал таких пар, у которых окисленная форма содержит кислород ( МпО -, CrOf -, Cr2O2 -, АзО3, ), возрастает, а с уменьшением концентрации ионов Н падает. [7]
При концентрации окислителя С2 на металле возможно установление двух стационарных потенциалов в пассивной или в активной областях. Пассивное состояние в этих условиях не будет самопроизвольно возобновляться. Другими словами, если в раствор с окислителем поместить активный металл, то он в этом случае не запассивируется. Если же металл предварительно будет запассивирован, то он сохранит пассивное состояние при погружении в такой раствор. Окислители с концентрацией С3 и С4 создают устойчивое пассивное состояние, причем скорость коррозии не будет зависеть от концентрации окислителя. При концентрации окислителя Съ скорость коррозии металла увеличивается вследствие того, что стационарный потенциал металла смещается в область перепассивации. [8]
Если концентрация окислителя низка и не обеспечивает плотности катодного тока, равного или большего плотности тока пассивации металла, то металл будет находиться в активном состоянии и коррозия его от увеличения скорости катодной деполяризации может даже возрастать. [9]
Контроль концентрации окислителя в водной фазе можно осуществлять периодически потенциометрическим титриметриче-ским методом ( см. разд. [10]
Повышение концентрации окислителя уменьшает толщину пленки, а также и потери металла от растворения. Это происходит по той причине, что при повышенном содержании окислителя возрастает скорость окисления металла в начале процесса, что в свою очередь приводит к быстрому обогащению окислами железа слоя жидкости на границе с металлом. Кристаллизация магнитной окиси из пересыщенного таким образом раствора ускоряется, число возникающих центров кристаллизации Fe3O4 увеличивается, а толщина образуемой пленки уменьшается. При малом содержании окислителя толщина пленки будет возрастать, но механическая прочность ее уменьшится. Получаемая пленка будет рыхлой и легко истирающейся. [11]
Равенство концентраций окислителя одной пары и восстановителя другой пары в этом случае имеется всегда. [12]
Уменьшение концентрации окислителей в растворе определяют потенциометрически. [13]
Равенство концентраций окислителя одной пары и восстановителя другой пары в этом случае имеется всегда. [14]
Определяют концентрацию окислителя или восстановителя, который медленно реагирует с соответствующим веществом в растворе. Определение основано на измерении скорости реакции. Смешивают испытуемый раствор с рабочим, взятым в значительном избытке. Через определенные промежутки времени определяют количество продукта реакции или количество прореагировавшего рабочего раствора. Составляют график, на оси абсцисс которого откладывают время, а на оси ординат результат определения. [15]
Страницы: 1 2 3 4