Концентрация - окислитель
Cтраница 2
Определяют концентрацию окислителя или восстановителя, который медленно реагирует с соответствующим веществом в растворе. Определение основано на измерении скорости реакции. [16]
Информация о концентрации окислителя в водной фазе реакционной среды является одновременно информацией и о реакционной способности органической фазы. [17]
 |
Кривые распределения.| Кривые распределения питтингов по глубине цля стали 1Х18Н9Т при различном времени воздействия электролита, содержащего 2 % пассиватора и 3 0 % активатора. [18] |
С увеличением концентрации окислителя кривые распределения в целом сдвигаются влево, за исключением первых ветвей, сдвигающихся вправо. Это указывает на то, что при увеличении концентрации окислителя процесс коррозии в большинстве точек замедляется и на поверхности остается лишь небольшое число активных центров ( - 2 - 3 %), в которых процесс развивается интенсивно. [19]
При повышении концентрации окислителя процесс формирования пленки магнитной окиси ускоряется и количество уходящего в раствор не связанного окисного железа Na2pe204 уменьшается, что в свою очередь задерживает образование налетов гидрата окиси железа. Понижение содержания окислителя способствует образованию красных налетов. В начальном периоде оксидирования, когда поверхность металла еще не успела закрыться защитной пленкой окисла и растворение металла происходит с наибольшей скоростью, тоже создаются благоприятные условия для выделения осадка гидрата окиси, так как реакция протекает слишком медленно для того, чтобы связать все образующееся окисное железо. Опасность появления красных окислов на оксидной пленке особенно велика в самом начале процесса. На практике детали вынимают из ванны через 2 - 3 мин. [20]
Если изменение концентрации окислителя контролируется оптическим методом, то лучше применять H2SO4, так как в этой среде молярный коэффициент погашения серебра ( П) наибольший. [21]
При увеличении концентрации окислителя от С1 до Съ его обрат-тимый потенциал становится более благородным в соответствии с уравнением Нернста. [22]
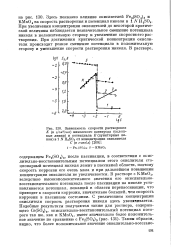 |
Зависимость скорости растворения К ( в г / см2 / час никелевого электрода ( сплошные линии и потенциала Е ( пунктирные линии в 1 N H2SO4 от концентрации окислителя С ( в г-вкв / л. [23] |
При увеличении концентрации окислителей до некоторой критической величины наблюдается незначительное смещение потенциала никеля в положительную сторону и увеличение скорости его растворения. При достижении критической концентрации окислителя происходит резкое смещение потенциала в положительную сторону и уменьшение скорости растворения никеля. [24]
В почве отношение концентраций окислителя и восстановителя редко бывает равно единице, а концентрация компонентов ОВ-системы в целом низкая. Этим и объясняется чрезвычайная податливость почвы к изменению и снижению величины ОВ-потенциала при увлажнении. Повышение содержания органического вещества в почве повышает ее буферность ( загруженность), поэтому все мероприятия, направленные на повышение содержания гумуса в почве, положительно сказываются на ее ОВ-состоянии. [25]
 |
Поверхностная диффузия.| Появление шероховатости на поверхности меди. [26] |
Но при некоторых концентрациях окислителя адсорбция происходит селективно. [27]
В зазорах средней величины концентрация окислителя снижается в меньшей степени и коррозия приобретает местный характер, проникая на относительно большую глубину. [28]
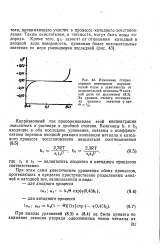 |
Изменение стационарного потенциала коррозионной пары в зависимости от относительной величины в анод -, ной доли по уравнению. За уровень отсчета потенциала принято значение р при. [29] |
Коррозионный ток пропорционален этой концентрации окислителя в растворе в дробной степени. [30]
Страницы: 1 2 3 4