Концентрация - пиридин
Cтраница 4
Метод основан на цветной реакции пиридина с реактивом, состоящим из уксусного ангидрида и лимонной кислоты. При наличии пиридина появляется розовая окраска. Чем больше концентрация пиридина, тем быстрее появляется окраска. [46]
Для того чтобы получить оптимальные концентрации как пиридина, так и основания, необходимо изменять их поочередно до тех пор, пока положение максимума не перестанет изменяться. Это обычно достигается тремя опытами, в которых изменяется концентрация пиридина, и тремя опытами, в которых изменяется концентрация четвертичного основания. Как оказалось, максимальное светопо-глощение получается для реагента, содержащего 70 % пиридина и являющегося 0 073 М по гидроокиси тетраэтиламмония. Закон Бера при этом выполняется, и, как было найдено, коэффициент вариации составляет 5 % для анализов, сделанных в один день. [47]
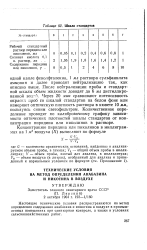 |
Шкала стандартов. [48] |
После нейтрализации пробы и стандартной шкалы объем жидкости доводят до 6 мл дистиллированной водгп. Через 20 мин сравнивают интенсивность окраски проб со шкалой стандартов на белом фоне или измеряют оптическую плотность раствора в кювете 10 мм, пользуясь синим светофильтром. Количественное определение проводят по калибровочному графику зависимости оптических плотностей шкалы стандартов от концентрации пиридина или пиколинов в растворе. [49]
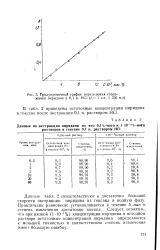 |
Градуировочный график определения содержания пиридина в 0 1 н. НС1 ( / 1 см, X 256 нм. [50] |
Данные табл. 2 свидетельствуют о достаточно большой скорости экстракции пиридина из гексана в водную фазу. Практически равновесие устанавливается в течение 5 мин и степень извлечения достаточно высока. Следует отметить, что при низкой ( 1 10 - 4 %) концентрации пиридина в исходном растворе остаточные концентрации пиридина определяются с меньшей точностью и соответственно степень извлечения имеет большую ошибку. [51]
Этот список будет увеличиваться по мере расширения наших знаний об органическом веществе вод; ( возможно, будут найдены показатели, еще более достоверные при прогнозе нефтегазоносности, чем перечисленные в нем. Так, например, вероятно, только недостаточное число определений бензола в разных районах, имевшихся в нашем распоряжении, а также разнобой в методиках его определения помешали нам присоединить его к числу наиболее достоверных показателей. Сказанное относительно недостаточного числа определений по отдельным районам относится и к соотношениям различных характеристик в угольных и хлороформных элюатах и к концентрациям пиридина и некоторых других компонентов, поведение которых по атой причине мы не рассматривали. [52]
Растворитель оказывает часто каталитическое действие, способствуя путем сольватации разделению ионов. Таким образом, растворитель благоприятствует спонтанной ионизации веществ в мономолекулярных реакциях и отрыву иона, отщепляющегося в переходном состоянии, при бимолекулярных реакциях. Примером может служить получение четвертичного производного пиридина при помощи бромистого метила в бензольном растворе ( о), когда прибавление метилового спирта ускоряет превращение, которое при этом начинает подчиняться кинетическому уравнению третьего порядка, так как скорость становится пропорциональной концентрации пиридина, бромистого метила и метилового спирта. Подобные эффекты часто наблюдаются при некоторых синхронных электронных переходах ( см. стр. [53]
Эквимолекулярные количества метилового спирта и трифенилхлорметана или трифенилбромметана реагируют в сухом бензоле в присутствии пиридина ( для связывания хлористого водорода), давая метил-трифенилметиловый эфир. В пределах ошибки опыта реакция с метанолом является реакцией третьего порядка. Если взять фенол вместо метанола, образуется фениловый эфир, но со скоростью в 50 раз меньшей. Реакция по-прежнему третьего порядка, хотя зависимость от концентрации пиридина показывает, что около половины фенола связано в комплексе пиридином. [54]
Кинетика реакций различных дипиридин-железо ( П) порфирино-вых комплексов с кислородом в водных и неводных растворителях изучена двумя группами исследователей. Као и Ванг [119] получили данные в пользу двух путей процесса. Меньшее значение имеет путь, включающий перенос электрона при столкновении несвязанного кислорода дипиридиновым комплексом железа. Основной вклад дает процесс, скорость которого обратно пропорциональна концентрации пиридина. [55]
Страницы: 1 2 3 4