Концентрация - исходный конечный продукт
Cтраница 1
Концентрации исходных и конечных продуктов этих реакций - А, В, D и Е - поддерживаются постоянными, тогда как концентрации двух промежуточных компонентов могут изменяться во времени. [1]
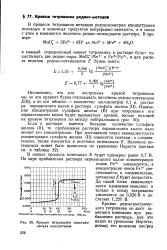 |
Кривая титрования восстано - ВИДНО из Уравнения Нернста, вителя окислителем. потому что величина окс / ред. [2] |
В процессе титрования методами редоксиометрии концентрации исходных и конечных продуктов непрерывно меняются, а в связи с этим и изменяется величина редокс-потенциалов раствора. [3]
 |
Кривая титрования восстановителя окислителем. [4] |
В процессе титрования по редокс-методу концентрации исходных и конечных продуктов непрерывно меняются, а в связи с этим и изменяется величина редокс-потенциала раствора. [5]
В состоянии равновесия устанавливается совершенно определенное соотношение между концентрациями исходных и конечных продуктов реакции. [6]
При окончательном определении потенциала восстановления аниона или нейтральной молекулы для данных условий необходимо учитывать концентрацию исходных и конечных продуктов реакции, что внесет некоторую поправку в найденную нами величину потенциала. [7]
Вместе с тем, следует учитывать возможность некоторого увеличения длительности реакции из-за уменьшения средней располагаемой разности концентрации исходных и конечных продуктов ( стр. Поэтому для полного использования потенциальных резервов производительности необходимо одновременно с переводом на непрерывный режим работы проведение технологических и конструктивных мероприятий по интенсификации самих реакционных процессов. [8]
Однако поскольку эти процессы имеют конечную скорость, то непосредственно у поверхности ионита может существовать слой раствора ( условно называемый диффузионным слоем) с концентрациями исходных и конечных продуктов процесса, отличающимися от их концентрации в объеме раствора. [9]
Определяющий критерий ( Sp ерКрт) отличается от критерия равновесности Q, полученного Дьяконовым, лишь тем, что в на-щем случае в этот критерий входят безразмерная степень суммарного превращения бр, объемная скорость подачи сырья Vp и время контакта т, тогда как критерий Q, по определению самого автора, характеризует меру отношения внутренних скоростей превращения и связь между концентрациями исходных и конечных продуктов превращения. Иными словами, критерий Q является отношением произведений констант скоростей и констант равновесия обратной и прямой реакции, имеющей определенный механизм, выраженный также определенными ( постулированными) стехио-метрическими коэффициентами и компонентами системы. [10]
При установившемся равенстве скоростей прямой и обратной реакций наступает химическое равновесие. Состояние химического равновесия характеризуется тем, что концентрация исходных и конечных продуктов реакции приданных температуре и давлении остается постоянной. Иными словами, при установлении равновесия в единицу времени образуется такое количество веществ D и Е, какое в это же время распадается с образованием веществ А и В. [11]
При установившемся равенстве скоростей прямой и обратной реакций наступает химическое равновесие. Состояние химического равновесия характеризуется тем, что концентрация исходных и конечных продуктов реакции при данных температуре и давлении остается постоянной. Иными словами, при установлении равновесия в единицу времени образуется такое количество веществ D и Е, какое в это же время распадается с образованием веществ А и В. [12]
Реакции этого типа обратимые, равновесные. Скорость прямой и обратной реакций зависит от соотношения концентраций исходных и конечных продуктов. Механизмы прямой и обратной реакций идентичны. [13]
Он характеризует отношение скоростей обратной и прямой реакции и связь между концентрациями исходных и конечных продуктов реакции. [14]
В кислых растворах ( при рН ниже 4) сероводород находится преимущественно в виде молекул, в щелочных растворах ( при рН выше 9) - в виде ионов. Скорость взаимодействия реагирующих между собой молекул сероводорода и кислорода подчиняется законам химической кинетики и зависит от концентрации исходных и конечных продуктов. [15]
Страницы: 1 2