Концентрация - анализируемый раствор
Cтраница 1
Концентрации анализируемого раствора и реактива должны быть высокими. [1]
 |
Кристаллы K2Pb [ Cu ( NO c ]. [2] |
Концентрации анализируемого раствора и раствора реактива должны быть высокими. [3]
Концентрации анализируемого раствора и реактива должны быть высокими. [4]
Концентрация анализируемого раствора не должна превышать 0 5 - 1 N по хлоридам и нитратам. Наиболее пригоден раствор, подкисленный серной кислотой. [5]
Концентрации анализируемого раствора и реактива должны быть высокими. [6]
Концентрации анализируемого раствора и раствора реактива должны быть высокими. [7]
Концентрации анализируемого раствора и реактива должны быть высокими. [8]
 |
Цилиндры колориметра сливания. [9] |
Сан - концентрация анализируемого раствора, Аан - высота слоя анализируемого раствора при уравненных окрасках, Сст - концентрация стандартного раствора, ficr - высота слоя стандартного раствора при уравненных окрасках. [10]
 |
Полное внутреннее отражение луча. а - предельный угол падении.| Принципиальная схема автоматического рсфракто. [11] |
При изменении концентрации анализируемого раствора луч света отклоняется в ту или иную сторону и равенство освещен-ностей фотосопротивлений нарушается. В результате на вход электронного усилителя ЭУ подается сигнал, знак и величина которого определяются отклонением концентрации контролируемого раствора от сравнительного. [12]
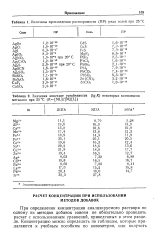 |
Величины произведения растворимости ( ПР ряда солей при 25 С.| Значения констант устойчивости ( lg К некоторых комплексов металлов при 25 С ( K [ ML ] / [ M ] [ L ]. [13] |
При определении концентрации анализируемого раствора по одному из методов добавок совсем не обязательно проводить расчет с использованием уравнений, приведенных в этом разделе. [14]
В отношении концентрации анализируемого раствора нужно сказать, что на основании теории ионного обмена раствор должен быть разбавленным, так как величина ионообменной емкости, приходящаяся на единицу объема зерен ионита, ограничена. В очень разбавленных растворах, однако, возникают процессы гидролиза, мешающие ионному обмену. Количественное поглощение обменивающихся ионов достигается даже при таких малых концентрациях, как 10 - 5 и 10 - 6 моля. При очень низких концентрациях трудно определять ионы, вытесняемые из колонки. В эти случаях применяют меченые ато: мы. Более концентрированные растворы рекомендуется разбавлять до этих концентраций. [15]
Страницы: 1 2 3 4 5