Концентрация - исходный реагент
Cтраница 3
Скорость химической реакции определяется как скорость уменьшения концентраций исходных реагентов или скорость увеличения концентраций продуктов. Для измерения скорости необходимо следить подходящим методом за изменением во времени концентрации исходного реагента или продукта. [31]
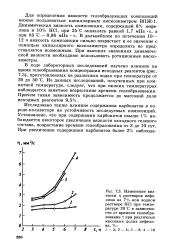
На рис. 4 а приводятся расчетные профили концентраций исходного реагента полученные в предположении что оус, ( 1 -) сг. Там же показаны экспериментальные данные для процессов окисления Зог и гидрохлорирования ацетилена. Как видно из рисунка, экспериментальные и расчетные профили сопоставимы. [32]
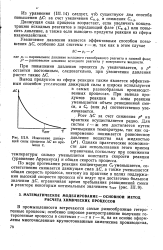 |
Изменение движу - давление вещества над жидкостью щей силы процесса ДС во вре - ( р. Однако практические возможно-мени т - сти для использования этого приема. [33] |
Движущая сила процесса возрастает, если увеличить концентрацию исходных реагентов в передающей фазе ( Сп. [34]
По мере работы элемента ( разряда) уменьшается концентрация исходных реагентов и растет концентрация продуктов реакции, поэтому в соответствии с уравнением Нернста ЭДС элемента уменьшается. Кроме того, возрастает поляризация элемента. Поэтому при разряде элемента напряжение его постепенно падает. Кривая изменения напряжения во времени в процессе разряда называется разрядной кривой элемента. Чем меньше меняется напряжение при разряде элемента, тем больше возможностей его применения. Емкость элемента - это количество электричества, которое источник тока отдает при разряде. Она определяется массой реагентов в элементе, их эквивалентом и степенью превращения. [35]
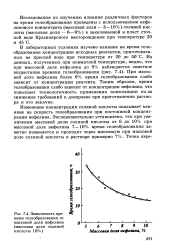 |
Зависимость времени гелеобразования от массовой доли нефелина ( массовая доля соляной кислоты 10 %. [36] |
В лабораторных условиях изучено влияние на время гелеобразования концентрации исходных реагентов, приготовленных на пресной воде при температуре от 20 до 50 С. При массовой доле нефелина более 9 % время гелеобразования слабо зависит от концентрации реагента. Таким образом, время гелеобразования слабо зависит от концентрации нефелина, что повышает технологичность применения композиции из-за снижения требований к дозировке при приготовлении раствора и его закачке. [37]
 |
Зависимость выхода продукта от температуры зажигания катализатора. [38] |
Температура зажигания определяется активностью катализатора, природой и концентрацией исходных реагентов. В процессе старения катализатора температура зажигания возрастает. [39]
Зависимость длины цепи и скорости образования свободных радикалов от концентрации исходных реагентов, их изменение в ходе реакции в связи с появлением продуктов окисления, изменением среды, состава свободных радикалов и их активности, обусловливает все многообразие кинетических законов, которые наблюдаются в процессах окисления органических соединений различных классов. [40]
В ходе лабораторных исследований изучено влияние на время гелеобразования концентрации исходных реагентов ( рис. 7.5), приготовленных на различных водах при температуре от 20 до 50 С. Из данных исследований, полученных при комнатной температуре, следует, что при низких температурах наблюдается заметное возрастание времени гелеобразования. [42]
При постоянной температуре наблюдаемая константа скорости не должна зависеть от концентраций исходных реагентов, поскольку в рамках принятой модели величина сж остается постоянной и зависит только от свойств растворителя. Получим общее выражение, определяющее температуру, при которой наблюдаемая константа скорости данной реакции имеет максимальное значение. [43]
Увеличение выхода продукта реакции за счет сдвига равновесия в результате повышения концентрации исходных реагентов также часто осуществляют на практике; обычно повышают концентрацию наиболее дешевого компонента. Так, при получении водорода конверсией СО водяным паром создают избыток паров воды, поскольку водяной пар относительно дешев. [45]
Страницы: 1 2 3 4 5