Концентрация - поверхностноактивное вещество
Cтраница 2
Согласно уравнению ( 94), время, при котором ток проходит через максимум, обратно пропорционально концентрации поверхностноактивного вещества в растворе. [16]
Это уравнение, согласно которому время ft, соответствующее полному покрытию поверхности электрода, обратно пропорционально квадрату концентрации поверхностноактивного вещества в растворе СА, является одновременно критерием, с помощью которого можно решить, какой из процессов определяет количество вещества, адсорбированного на поверхности капельного электрода. [17]
Это уравнение, согласно которому время &, соответствующее полному покрытию поверхности электрода, обратно пропорционально квадрату концентрации поверхностноактивного вещества в растворе СА, является одновременно критерием, с помощью которого можно решить, какой из процессов определяет количество вещества, адсорбированного на поверхности капельного электрода. [18]
Чтобы написать явное выражение для сил, нужно совершенно так же, как это было сделано в § 73 для случая стационарного движения капли, выразить концентрацию поверхностноактивного вещества через скорость движения жидкости. [19]
В основу наиболее простого и широко распространенного метода определения ККМ положено достаточно резко выраженное изменение цвета растворов, содержащих, кроме поверхностноактивного вещества, подходящий краситель, которое происходит при достижении критического значения концентрации поверхностноактивного вещества. Коррин и Харкинс [16], ион ионизированного индикатора должен иметь заряд, противоположный заряду мицелл поверхностноактивного вещества. Кроме того, краситель должен существовать в растворе в виде равновесной смеси двух форм, одна из которых может избирательно солюбилизироваться мицеллами. [20]
С а, нас - дифференциальная емкость электрода, когда его поверхность полностью покрыта адсорбированным веществом; Cd) B - дифференциальная емкость электрода в отсутствие адсорбированного вещества; Cd - дифференциальная емкость электрода при концентрации поверхностноактивного вещества, меньшей, чем концентрация, соответствующая полному покрытию поверхности. Все значения емкостей должны быть измерены при одном и том же потенциале. [21]
Максимальная интенсивность процессов разрушения и ползучести полиэтилена, наблюдаемая в растворе NaOH, по всей вероятности, связана с изменением величины поверхностного натяжения, которое в соответствии с имеющимися данными проходит через экстремальное значение ( минимум) по мере роста концентрации поверхностноактивного вещества. В серной кислоте этот процесс замедляется с увеличением концентрации. [22]
Сначала рассмотрим случай, когда скорость адсорбции очень велика, так что лимитирующим процессом является диффузия. Если концентрация поверхностноактивного вещества в растворе мала и в равновесном состоянии не вся поверхность электрода покрыта адсорбированными частицами, то расчет зависимости степени заполнения поверхности электрода поверхностноактивным веществом в от времени [66] приводит к очень сложным выражениям. Расчеты сильно упрощаются, если предположить, что концентрация поверхностноактивного вещества достаточно велика для того, чтобы в равновесном состоянии поверхность электрода была полностью покрыта адсорбированными частицами. В этом случае при большой скорости адсорбции и достаточно малой скорости десорбции можно считать, что до времени полного покрытия электрода концентрация поверхностно-активных молекул у его поверхности значительно меньше, чем их концентрация в объеме раствора. [23]
Сначала рассмотрим случай, когда. Если концентрация поверхностноактивного вещества в растворе мала и в равновесном состоянии не вся поверхность электрода покрыта адсорбированными частицами, то расчет зависимости степени заполнения поверхности электрода поверхностноактивным веществом 6 от времени [66] приводит к очень сложным выражениям. Расчеты сильно упрощаются, если предположить, что концентрация поверхностноактивного вещества достаточно велика для того, чтобы в равновесном состоянии поверхность электрода была полностью покрыта адсорбированными частицами. В этом случае при большой скорости адсорбции и достаточно малой скорости десорбции можно считать, что до времени полного покрытия электрода концентрация поверхностно-активных молекул у его поверхности значительно меньше, чем их концентрация в объеме раствора. [24]
При повышении концентрации адсорбирующегося на электроде вещества прогибы на полярографических кривых увеличиваются до тех пор, пока ток не достигает величины нормального предельного тока; максимум остается подавленным вплоть до потенциала десорбции. Зависимость тока максимума от логарифма концентрации поверхностноактивного вещества имеет S-образную форму; следовательно, наибольшее изменение высоты максимума при добавлении в раствор поверхностноактивного вещества наблюдается тогда, когда максимум подавлен наполовину. [25]
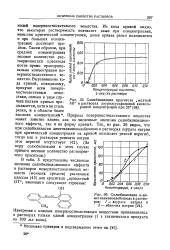 |
Солюбилизация красителя. желтый АВ в растворах лаурилсульфоновой кислоты.| Солюбилизация п-ди-метиламиноазобензола в растворах. / - лаурата натрия и 2-абиетата натрия. [26] |
Из хода кривой видно, что некоторая растворимость возникает даже при концентрациях, меньших критической концентрации, далее кривая резко поднимается и при больших концентрациях достигает предела. Таким образом, при средних концентрациях весовое количество растворяющегося красителя почти прямо пропорционально концентрации поверхностноактивного вещества. [27]
Раньше уже было рассмотрено влияние поверхностноактивных веществ на реакцию, которая протекает только в одном направлении. В данном случае степень подавления тока зависит от потенциала, поэтому наблюдается сдвиг волны к отрицательным потенциалам при увеличении концентрации поверхностноактивного вещества. [28]
Сначала рассмотрим случай, когда скорость адсорбции очень велика, так что лимитирующим процессом является диффузия. Если концентрация поверхностноактивного вещества в растворе мала и в равновесном состоянии не вся поверхность электрода покрыта адсорбированными частицами, то расчет зависимости степени заполнения поверхности электрода поверхностноактивным веществом в от времени [66] приводит к очень сложным выражениям. Расчеты сильно упрощаются, если предположить, что концентрация поверхностноактивного вещества достаточно велика для того, чтобы в равновесном состоянии поверхность электрода была полностью покрыта адсорбированными частицами. В этом случае при большой скорости адсорбции и достаточно малой скорости десорбции можно считать, что до времени полного покрытия электрода концентрация поверхностно-активных молекул у его поверхности значительно меньше, чем их концентрация в объеме раствора. [29]
Сначала рассмотрим случай, когда. Если концентрация поверхностноактивного вещества в растворе мала и в равновесном состоянии не вся поверхность электрода покрыта адсорбированными частицами, то расчет зависимости степени заполнения поверхности электрода поверхностноактивным веществом 6 от времени [66] приводит к очень сложным выражениям. Расчеты сильно упрощаются, если предположить, что концентрация поверхностноактивного вещества достаточно велика для того, чтобы в равновесном состоянии поверхность электрода была полностью покрыта адсорбированными частицами. В этом случае при большой скорости адсорбции и достаточно малой скорости десорбции можно считать, что до времени полного покрытия электрода концентрация поверхностно-активных молекул у его поверхности значительно меньше, чем их концентрация в объеме раствора. [30]
Страницы: 1 2 3