Концентрация - исходное вещество
Cтраница 2
Если концентрации исходных веществ различны, то для выделения частного порядка реакции по одному из компонентов VA, VB... [16]
Сначала концентрации исходных веществ А и В максимальны; скорость прямой реакции v также будет максимальной, с уменьшением концентраций веществ А к В она будет убывать. По мере роста концентраций веществ С и D скорость у2, равная вначале 0 ( нулю), будет возрастать. [17]
Если концентрация исходного вещества меньше определенной, критической, то процесс протекает в кинетической области, с малым разогревом. При концентрациях, превышающих критическую, реакция в первых слоях должна идти в диффузионной области, с большим разогревом, с переходом в последующих слоях в кинетическую область и малым разогревом. [18]
Измерены концентрации исходного вещества в различные моменты времени. [19]
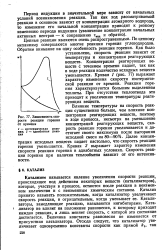 |
Зависимость скорости реакции горения от времени. [20] |
Далее концентрация исходных веществ падает настолько, что скорость реакции горения уменьшается. Кривая 2 выражает характер изменения скорости реакции горения в адиабатных условиях. Скорость реакции горения при наличии теплообмена зависит от его интенсивности. [21]
Если концентрации исходных веществ различны, то для выделения частного порядка реакции по одному из компонентов VA, VB - - используется метод изолирования Оствальда с последующим определением v - одним из рассмотренных способов. [22]
Увеличение концентрации исходных веществ приводит к смещению равновесия в сторону образования продуктов реакции, а увеличение концентрации продуктов реакции приводит к смещению равновесия в сторону образования исходных веществ. [23]
Расчет концентраций исходного вещества по секциям каскада для обратимых реакций производится последовательным решением приведенных в табл. П-12 уравнений, начиная с заданной концентрации. [24]
 |
Влияние повышения концентрации Св и коэффициента избытка ав вещества И на степень превращения вещества А и выход продукта D по веществу А в реакции А В та D. [25] |
Влияние концентрации исходных веществ на протекание гомогенных процессов наиболее существенно для параллельных и последовательных реакций с разными порядками основной и побочной реакций. [26]
Изменение концентраций исходных веществ во времени удовлетворительно описывается уравнением реакции первого порядка. В табл. 1 - 5 приведены Кэфф всех стадий реакции гидролиза меламина. [27]
Увеличение концентрации исходного вещества или уменьшение концентрации продукта реакции ( отвод его из сферы реакции) вызывает смещение равновесия в сторону прямой реакции. [28]
Увеличение концентрации исходного вещества или уменьшение концентрации продукта реакции ( отвод его из сферы реакции) вызывает смещение равновесия в сторону прямэй реакции. [29]
Зная концентрацию исходного вещества в объеме, нанесенном на хроматограмму ( обычно 0 01 мл), нетрудно рассчитать процентное содержание исследуемых веществ в смеси. Широко распространен также анализ полученных растворов при помощи спектрофотометра, что значительно сокращает сроки проведения исследования и дает точные результаты. [30]
Страницы: 1 2 3 4