Концентрация - исходное вещество
Cтраница 4
Значительное изменение концентрации исходных веществ Си, Сн может привести к замене одного лимитирующего этапа процесса другим. [47]
 |
Влияние концентрации катализатора Скаг ( кривая / и активатора Са ( кривая 2 на константу скорости каталитической реакции. [48] |
Значительное изменение концентрации исходных веществ Си, Си может привести к замене одного лимитирующего этапа процесса другим. [49]
Для каких реакций концентрация исходного вещества всегда линейно уменьшается со временем. [50]
 |
Снижение энергии. [51] |
Скорость реакции пропорциональна концентрации исходного вещества и катализатора. [52]
Экспериментально можно определить концентрации исходных веществ в различные моменты времени. [53]
CA U - концентрации исходных веществ и продуктов, выраженные в молях на литр. [54]
В диффузионной области концентрация исходного вещества в центре зерна равна нулю. Следовательно, параметр в равен максимальной безразмерной температуре разогрева во виутридиффу-зионной области. Если перенос тепла осуществляется только путем молекулярной диффузии в порах частицы и справедливо равенство ( III. [55]
Индекс 1 при концентрации исходного вещества для простоты опускаем. [56]
В начале процесса концентрация исходных веществ - СО и Н2О велика и поэтому значительна скорость прямой реакции. Но по мере протекания процесса окись углерода и водяные пары расходуются, концентрация их уменьшается и прямая реакция постепенно замедляется. Одновременно увеличивается количество полученных продуктов ( водорода и углекислого газа), растет их концентрация, а потому повышается и скорость обратной реакции. Наконец, наступает такой момент, когда скорости прямой и обратной реакции становятся равными. Такое состояние реагирующей системы называется химическим равновесием. [57]
В начале процесса концентрация исходных веществ - СО и Н2О велика и поэтому значительна скорость прямой реакции. Но по мере протекания процесса окись углерода и водяные пары расходуются, концентрация их уменьшается и прямая реакция постепенно замедляется. Одновременно увеличивается количество полученных продуктов ( водорода и углекислого газа), растет их концентрация, а потому повышается и скорость обратной реакции. Наконец, наступает такой момент, когда скорости прямой и обратной реакций становятся равными. Такое состояние реагирующей системы называется химическим равновесием. [58]
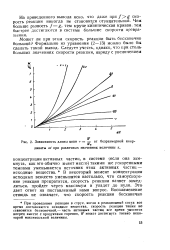 |
Зависимость длины цепи ч - - от безразмерной коор. [59] |
В некоторый момент концентрация исходных веществ уменьшится настолько, что самоускорение реакции прекратится, скорость реакции начнет замедляться, пройдет через максимум и упадет до нуля. Эта дает ответ на поставленный нами вопрос. [60]
Страницы: 1 2 3 4
