Концентрация - другое вещество
Cтраница 1
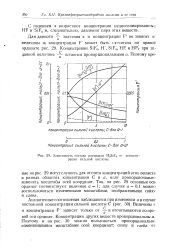 |
Зависимость состава растворов H2SiF6 от концентрации сильной кислоты. [1] |
Концентрации других веществ пропорциональны а. [2]
Определим изменение концентраций других веществ. В соответствии с уравнением реакции на получение d молей вещества D расходуется а молей вещества А и b молей вещества В. Соответственно на получение молей вещества D расходуется xald вещества: А и xb / d вещества В. [3]
Величина поляризации для неполярных веществ практически не зависит от концентрации других веществ в системе и температуры, а для полярных веществ зависит от этих параметров. [4]
В этом случае i д также не зависит от концентрации других веществ, так как они могут быть здесь только нейтральными веществами. [5]
Достаточно знать изменение во времени концентрации одного вещества, так как концентрация других веществ определяется стехиометрическими коэффициентами уравнения реакции. [6]
Если при бимолекулярной реакции концентрация одного из исходных веществ значительно больше концентрации другого вещества, то во время реакции концентрация вещества, взятого в избытке, остается практически постоянной. [7]
В этой схеме Q - константа скорости образования деполяризатора А, которая может зависеть от концентрации других веществ, участвующих в этой химической реакции. [8]
Здесь константа ku ( равная г / [ О2 ] 2) может также зависеть от концентрации других веществ, таких, как ионы 5Оз -, катализатор и ионы водорода. Эта концентрация примерно отвечает концентрации кислорода в чистой воде в условиях равновесия с чистым кислородом, находящимся при давлении 0 061 МПа и комнатной температуре. При более высоких концентрациях кислорода скорость реакции, очевидно, имеет первый порядок. Примеси, присутствующие в следовых количествах, могут оказывать значительный эффект. [9]
В в зону эффективного действия межмолекулярных сил пропорциональна коэффициенту реакции и концентрации вещества В и не зависит от концентрации других веществ. [10]
Исследуемый объект часто представляет собою очень сложное по составу вещество, в котором концентрация определяемого элемента очень мала, а концентрация других веществ ( основы) довольно велика. Вместе с рядом других обстоятельств это приводит к заметным колебаниям в параллельных определениях. Поэтому при определениях малых концентраций допускаются относительно большие ошибки, 10 и больше процентов. [11]
Океаны являются по существу неисчерпаемой кладовой большого числа ценных металлов, однако концентрации этих металлов чрезвычайно малы по сравнению с концентрациями других веществ, растворенных в морской воде. Несмотря на это, по меньшей мере один из металлов, магний, извлекается из морской воды с помощью обычных способов химической технологии. [12]
Однако концентрация катализатора-ионов водорода - не, изменяется в ходе реакции, а концентрация воды в водном растворе велика по сравнению с концентрациями других веществ. В результате меняется только концентрация сахара и реакция оказывается псевдопервого порядка. [13]
Однако концентрация катализатора - ионов водорода - не изменяется в входе реакции, а концентрация воды в водном растворе велика по сравнению с концентрациями других веществ. [14]
Для слабых концентраций материалов в реакторе вероятность того, что молекула вещества А попадает в зону эффективного действия межмолекулярных сил, пропорциональна коэффициенту КАВ реакции и концентрации вещества Л и не зависит от концентрации других веществ. [15]
Страницы: 1 2 3