Концентрация - другое вещество
Cтраница 2
Из выражений ( 5 - 23) и ( 5 - 25) для скоростей реакции выше первого порядка следует, что если в смеси содержится небольшое количество одного из реагирующих веществ, то изменение концентраций других веществ в ходе реакции может быть относительно небольшим. Поэтому в этом случае реагирование можно рассматривать как процесс первого порядка относительно вещества, находящегося в недостатке. [16]
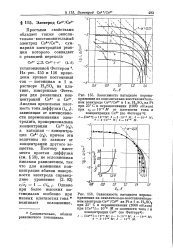
Анодная предельная плотность тока диффузии ( гд 3), зависящая от интенсивности перемешивания электролита, пропорциональна концентрации Се3 ( с3), а катодная - концентрации Се4 ( с4), причем эти величины не зависят от концентрации другого вещества. [18]
Скорость реакции аксиального изомера можно положить & а [ А ] [ Р ], где ka - константа удельной скорости реакции аксиального изомера, [ А ] - его концентрация и [ Р ] - фактор, определяющий концентрацию других веществ, входящих в кинетическое уравнение. [19]
Для реакции RCHCH2 C12 - RCHC1 - CH2C1, катализируемой FeCIs, выведите кинетическое уравнение, если известно, что скорость лимитируется превращением я-комплекса в а-комплекс, одновременно протекает некаталитическая реакция, а концентрации промежуточных комплексов так малы, что ими можно пренебречь по сравнению с концентрациями других веществ. [20]
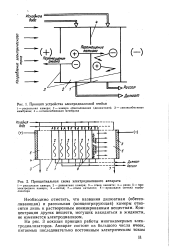 |
Принцип устройства электродиализной ячейки.| Принципиальная схема электродиализного аппарата. [21] |
Необходимо отметить, что названия дилюатная ( обессоливающая) и рассольная ( концентрирующая) камеры относятся лишь к растворенным ионизированным веществам. Концентрация других веществ, могущих находиться в жидкости, не изменяется электродиализом. [22]
Фундаментом химической кинетики является закон действия масс, при идеальном соблюдении которого в разбавленных растворах скорость любой химической реакции пропорциональна произведению - концентраций веществ действительно участвующих в реакции. Она не зависит ни от концентраций других веществ, ни от наличия или отсутствия других реакций. Если вещество может реагировать само с собой, то, согласно этому закону, скорость реакции будет пропорциональна квадрату, кубу или даже более высоким степеням концентрации такого вещества. В частности, прямая и обратная реакции обратимого процесса являются независимыми, а суммарная скорость обратимой реакции равна разности скоростей прямой и обратной реакции. [23]
В присутствии небольшого количества посторонних ионов в растворе связь между предельной плотностью тока диффузии гд j и концентрацией Cj становится сложнее, однако пропорциональность между iRj и Cj в основном сохраняется. При этом гд, до некоторой степени зависит от величин концентраций других веществ Ck Ф j даже в отсутствие химического равновесия. [24]
Кроме расхождений, связанных с прибором, могут иметь место действительные изменения величины поглощения света веществом из-за взаимодействия анализируемого вещества с растворителем и другими веществами. Изменение е при этом может быть весьма существенным и его точное значение оказывается зависимым от концентрации других веществ в анализируемой пробе. [25]
Приборы, основанные на интерферометрическом методе используют в качестве лабораторных и переносных газоанализаторов. Они нашли применение не только для определения концентрации молекулярного водорода, но и для определения концентрации других веществ, например, метана и диоксида углерода. [26]
Поэтому для того, чтобы растворы реагировали между собой в одинаковых объемах, необходимо выразить концентрацию другого вещества в моль эквивалентах на литр. [27]
HJ различны, то и их смещение вдоль оси X будет происходить на различное расстояние. Иначе говоря, если мы зафиксируем какую-либо концентрацию, например i, и будем следить за ее движением, то заметим, что сопутствующие ей концентрации других веществ непрерывно изменяются. [28]
В реакции принимают участие несколько веществ. Чтобы судить о развитии реакции во времени, достаточно проследить за изменением концентрации одного из них. Изменение концентраций других веществ происходит в соответствии с изменением одного из компонентов, так как количества молей реагирующих веществ связаны между собою стехиометрическим уравнением реакции. [29]
Купаетесь ли вы в ледяной воде или играете в мяч на горячем солнце, температура тела редко отклоняется от 37 С больше, чем на градус. Точно так же рН крови поддерживается постоянным, как и концентрация других веществ в крови и в клетках. Ваше теле быстро вышло бы из строя при нарушении химического баланса. [30]
Страницы: 1 2 3