Концентрация - соль - железо
Cтраница 2
При использовании для травления проката в 20 %: ной HaS04 ингибитор не выпадает в осадок до концентрации солей железа 5 г / л, совмещается с пенообразователями, дает гладкую поверхность. При работе ванн травления с ингибитором ПГУ-2 существенно снижается расход кислоты, увеличивается время их работы в 1 5 - 1 7 раза ингибитор на 90 % защищает сталь от перетрава. [16]
 |
Расчетная псевдостационарная концентрация электролита по С Ме. [17] |
Этот электролит через 2 - 3 смены, с учетом специфики данного производства, быстро приобретает псевдостационарное состояние по концентрации соли железа. Кроме того, раствор с такой концентрацией соли железа имеет зоны наивысшей электропроводности и наименьшей вязкости, покрытия, полученные из него, отличаются наибольшей работоспособностью. [18]
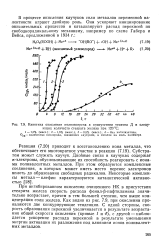 |
Кинетика окисления полиизопрена в присутствии неозона Д и следующих количеств стеарата железа при 120 С. [19] |
При ингибированном окислении очищенного НК в присутствии стеарата железа скорость расхода фенил - ( 5-нафтиламина значительно возрастает, причем в тем большей степени, чем выше концентрация соли железа. Как видно из рис. 7.9, при окислении проявляются две конкурирующие тенденции. С одной стороны, скорость образования перекисей увеличивается в результате возрастания общей скорости окисления ( кривые / и 4), с другой - наблюдается ускорение распада перекисей в результате уменьшения энергии активации их разложения под влиянием ионов поливалентных металлов. [20]
 |
Влияние времени контакта на связывание хлора и образование коагулянта ( Концентра-пия хлора в воде до растворения 2 0667 г / л. Отношение веса стружки к объему растворителя 1. 20. [21] |
Оптимальная концентрация хлорной воды, подаваемой на насадкудля коррозии, была установлена рядом опытов, которые показали, что при всех плотностях насадки повышение концентрации хлорной воды приводит к увеличению концентрации солей железа. До концентрации хлорной воды 1 7 г / л содержание хлорного железа в растворе прямо пропорционально концентрации активного хлора. [22]
Для определения по номограмме содержания кислоты в травильном растворе точку на шкале удельного веса, соответствующую удельному весу данного раствора, соединяют прямой линией с точкой, соответствующей данному раствору на шкале концентрации соли железа. Точка пересечения этой прямой со шкалой содержания кислоты укажет концентрацию свободной кислоты в данном растворе. [23]
Ферроцианид калия дает белый осадок ферроцианида железа ( II) - FeJFe ( CN) 6 ] или ферроцианида калия и железа ( И) - K2Fe [ Fe ( CN) 6 ], в зависимости от концентрации соли железа и реактива. [24]
Ферроцианид калия дает белый осадок ферроцианида железа ( II) - Fe [ Fe ( CN) 6 ] или ферроцианида калия и железа ( II) - K2Fe [ Fe ( CN) 6 ], в зависимости от концентрации соли железа и реактива. [25]
Ферроцианид калия дает белый осадок ферроцианида железа ( II) - Fe [ Fe ( CN) 6 ] или ферроцианида калия и железа ( II) - K2Fe [ Fe ( CN) e ], в зависимости от концентрации соли железа и реактива. [26]
 |
Влияние Дк и Сме на Нм покрытий ( НС11 5 г / л, t76 C. [27] |
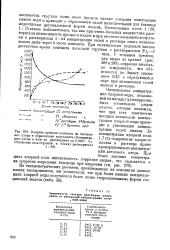
Влияние - Сме на Ям покрытий. Изменение концентрации соли Железа в растворе изменяет условия осаждения железа за счет изменения поляризации катода [10], а это сказывается, в свою очередь, и на величине Ям покрытий. [28]
 |
Зависимость свойств сплава N1 - Fe от соотношения концентрации сульфа-мииоаокислых солей иикели и железа а электролите. [29] |
С увеличением относительной концентрации солей железа в электролите возрастает концентрация железа cFe в сплаве. С увеличением концентрации соли железа в электролите резко возрастают напряжения в покрытии о. Если электролит содержит более 100 г / л Fe ( NH2SO8) 2, то не удается получить пластичные, отслаивающиеся от основы осадки; поэтому в электролит вводят 2 г / л сахарина. [30]
Страницы: 1 2 3