Концентрация - соль - никель
Cтраница 1
Концентрация соли никеля и в кислом, и в щелочном растворах мало влияет на скорость процесса. Увеличение концентрации гипофосфита в щелочном растворе оказывает существенное влияние на скорость процесса, однако, в кислых растворах увеличение скорости процесса обнаруживается лишь в случае поддержания оптимального соотношения между концентрациями гипофосфита и буферирующего соединения. [1]
Вследствие аномального соосаждения металлов группы железа концентрация солей никеля обычно в 10 - 30 раз превышает концентрацию солей железа. Борная кислота играет роль буфера; кроме того, она способствует уменьшению коэрцитивной силы покрытий. Соли калия, натрия, магния добавляют для увеличения проводимости раствора. Сахарин вводят для снижения внутренних напряжений в сплаве и получения равномерных покрытий. [2]
Максимальное значение скорости реакции при изменении концентрации солей никеля соответствует 100 Г / л сернокислого никеля. [3]
Для скорого наращивания никеля рекомендуется повышение концентрации соли никеля, уменьшение концентрации или даже полное изъятие проводящих солей и замена щелочных хлоридов хлоридом никеля. Помимо того, снижается величина рН и повышается температура. [4]
Как видно из таблицы, электролиты отличаются по концентрации соли никеля, температуре и применяемой плотности тока. Первый электролит в таблице предложен для применения в полиграфии, остальные электролиты используются в производстве для наращивания матриц и точных изделий в зависимости от материала формы и необходимости интенсификации процесса. [5]
В процессе пассивирования никелевых анодов трудно поддерживать постоянный состав электролита, так как концентрация солей никеля в нем непрерывно падает. Поэтому при никелировании принимаются все меры для того, чтобы уменьшить или предотвратить вовсе пассивирование анодов. К числу подобных мероприятий относится некоторое увеличение анодной поверхности, что снижает анодную плотность тока и, следовательно, величину анодной поляризации, а также введение специальных активаторов, на действии которых мы уже останавливались. [6]
Концентрацию комплексообразующих веществ устанавливают в зависимости от их природы, значения рН раствора и концентрации соли никеля. Цитраты и тартраты применяют обычно при низких температурах и низких концентрациях ионов ОН - и металла. [7]
Для каждой рецептуры никелевых электролитов устанавливается свое оптимальное значение рН, в соответствии с концентрацией солей никеля в электролите и применяемой плотностью тока. Выход же металла по току в никелевых электролитах при данной их кислотности повышается с плотностью тока до определенного предела, после которого, в результате сильного обеднения прикатодного слоя ионами никеля, выход металла по току приближается к нулю. [8]
Защитная способность никелевых покрытий, полученных из разбавленных по металлу комплексных электролитов, зависит от концентрации соли никеля, ионов хлора, рН электролита, катодной плотности тока и режима электролиза. Имеет место оптимальный состав электролита и режим электролиза, позволяющие получать беспористое немеловое покрытие толщиной 6 - 9 мкм. [9]
Основные трудности, которые пока препятствуют более широкому применению химического никелирования, это изменение состава раствора во время работы, в результате чего уменьшается концентрация солей никеля и гипофосфита, накопление фосфита никеля и выпадение его в осадок, что вызывает возрастание кислотности раствора и снижение скорости выделения никеля вплоть до полного прекращения процесса. Если не принимать специальных мер по корректированию и регенерации раствора для никелирования, то после каждой загрузки его следует заменять свежим. На каждый грамм осажденного никеля расходуется 5 - 6 г гипофосфита. На некоторых заводах [389] в ванну добавляют определенное количество 1 5 % - ного раствора NaOH через каждые 20 - 25 мин. Для получения толстых покрытий ( 25 мк и выше) никель осаждают последовательно в нескольких ваннах. [10]
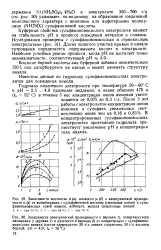
При введении ионов никеля в раствор образуется никелевое покрытие. С увеличением концентрации соли никеля скорость процесса возрастает ( см. рис. 18, кривая /, 2), а затем становится постоянной. Такого рода изменения скорости и потенциала связаны со скоростью диффузии ионов никеля к поверхности. [11]
Это связано, в частности, с подавлением снижения рН, происходящего при восстановлении никеля, за счет образования диметиламина и борной кислоты. Количество добавляемых буферных веществ, зависящее от концентрации соли никеля, обычно составляет 1 - 3 моля на 1 моль соли. [12]
Зависимости на рис. 75 позволяют выбрать соотношение концентраций солей никеля и кобальта в электролите для получения сплавов с заданными характеристиками. [13]
В концентрированных сульфаминовокислых электролитах протеканию гидролиза препятствует увеличение рН и концентрации соли никеля. [15]
Страницы: 1 2