Концентрация - тиосульфат
Cтраница 2
Некоторые из них содержат данные для регулирования концентрации тиосульфата натрия с целью согласования свойств обрабатывающего раствора со свойствами используемого фотоматериала. [16]
Таким образом, при стоянии раствора постепенно увеличивается концентрация тиосульфата и уменьшается концентрация сульфидов. Полисульфиды широко применяются для получения тиосульфата и сернистых красителей. В полисульфиде определяют содержание Na2S, Na2S2O3, общее содержанию серы, и щелочность. [17]
Эта скорость не зависит в таком случае от концентрации тиосульфата и пропорциональна произведению концентраций персульфата и комплексного аниона. [18]
Что происходит с растворимыми примесями по мере повышения концентрации тиосульфата натрия в упариваемом растворе. [19]
Теперь начертите график: как зависит скорость реакции от концентрации тиосульфата. [20]
Скорость растворения AgBr зависит в основном от температуры и концентрации тиосульфата. [21]
 |
Зависимость удельной скорости массопероноса N бензойной кислоты от ее начальной концентрации в иаобутаноле и начальной концентрации едкого натра в воде. [22] |
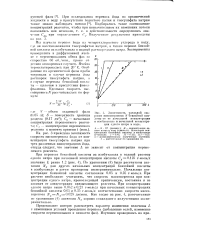
На рис. 3 приведена зависимость скорости массопереноса йода от концентрации тиосульфата натрия при трех различных концентрациях йода, откуда следует, что значение L не зависит симого реагента. [23]
Зависимость скорости реакции между тиосульфатом натрия и серной кислотой от концентрации тиосульфата изобразить графически, отложив концентрацию в молях на литр по оси абсцисс, а скорость реакции - по оси ординат. Скорость выразить как величину обратную времени, в течение которого в пробирках появляется слабая муть после смешения растворов. [24]
Этот эксперимент нужен был для того, чтобы выявить влияние концентрации тиосульфата натрия на скорость реакции с соляной кислотой. Полученный результат дает основание предположить, что и в ббщем случае одним из факторов, влияющим на скорость химической реакции, является концентрация реагирующих веществ. [25]
 |
Схема трехэлектрод-ной ячейки Эмерта. [26] |
Затем такой же объем рабочего раствора подвергается озонированию, вследствие чего концентрация тиосульфата в растворе изменяется в соответствия с реакцией ( VIII-2), после чего прореагировавший раствор также подвергается электролизу до момента появления тока в измерительной цепи. Разность времени холостого опыта ( без озонирования) и опыта с озонированным раствором ( At) пропорциональна концентрации озона в газе. [27]
С увеличением щелочности до 20 - 30 г / л VaOH я концентрации тиосульфата до 3 г / л наблюдается тенденция к уменьшению коррозии как стали, такУвполно приемлемый соотношением тиосульфата и щелочи является 0 5 г / л / / а, ) 0 и 2 г / л VaOH. Скорость коррозии ори асом составляет: для стали. [28]
Выделяющаяся сера вызывает помутнение раствора, наступающее тем быстрее, чем больше концентрация тиосульфата и чем выш температура раствора. [29]
По первому способу из системы циркуляции рабочего раствора выводят часть, кипячением упариваемую до концентрации тиосульфата натрия 650 - 700 г. л и затем охлажденную до 28 С. В результате этих операций выпадает осадок тиосульфата натрия, центрифугированием отделенный от маточного раствора, который возвращают в рабочую систему. [30]
Страницы: 1 2 3 4