Концентрация - титан
Cтраница 1
Концентрация титана, наиболее удобная для колориметрирования, равна 0 03 - 0 3 мкг / мл. [1]
При концентрации титана 4 5 мг / л ощущается кисловатый вяжущий привкус интенсивностью в 2 балла; концентрация 12 5 мг / л снижает прозрачность воды. [2]
Светопоглощение растворов пропорционально концентрации титана в пределах 5 - 200 мкг Ti в 50 мл. Определению мешают UVI и Fem, образующие с хромотроповой кислотой соединения, окрашенные соответственно в бурый и зеленый цвета. [3]
Скорость полимеризации пропорциональна концентрации четыреххлорн-стого титана и не зависит от количества металлалкила. Однако при использовании большого избытка дибутилцинка и малых количеств четырех-хлористого титана полимеризация замедляется. [4]
На оси абсцисс откладывают концентрации титана в мг, а на оси ординат - соответствующие им оптические плотности. [5]
В разбавленных растворах с концентрацией титана порядка 0 01 - 0 001 мкг / мл определение его дихлорхромотропо-вой кислотой возможно после предварительного концентрирования, например, экстракцией или соосаждением с бесцветными органическими соосадителями. [6]
Интенсивность этой окраски, пропорциональную концентрации титана, можно определить визуально или с помощью фотоколориметра с применением синего или светло-фиолетового светофильтра. Поскольку соли трехвалентного железа, присутствующие в растворе, также придают ему желтую окраску, мешающую колориметрированию титана, для обесцвечивания добавляют орто-фосфорную кислоту. [7]
Полученный график используют для определения концентрации титана в испытуемых растворах анализируемых проб. [8]
Вместо расчета по формуле находят концентрацию титана в испытуемом растворе по градуировочному графику зависимости оптической плотности от концентрации. [9]
Отклонение зависимости высоты полярографической волны от концентрации титана от прямолинейной при Т11т ], 0 4 М и исчезновение при этих концентрациях полярографического максимума на вольт-амперных кривых позволяет считать эту концентрацию граничной для образования полиномов в растворе. [10]
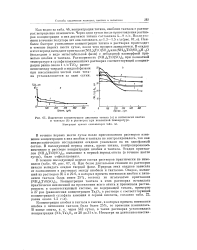 |
Изменение концентрации двуокиси титана ( а и пптиокисей ниобия и тантала ( Ъ в растворах при комнатной температуре. [11] |
Как видно из табл. 46, концентрация титана, ниобия и тантала в растворах непрерывно изменяется. Наиболее быстрое уменьшение концентрации титана в растворах происходит в течение первых шести суток, после чего процесс замедляется. Растворимость ( NH4) 2TiO ( SO4) 2 при комнатной температуре в сульфатноаммонийных растворах соответствующей концентрации равна около 1 г / л ТЮ2; равновесие между твердой и жидкой фазами при высаливании чистой соли титана устанавливается за одни сутки. [12]
Исследовано влияние на поляризацию насыпного анода концентрации растворенного титана в электролите и плотности тока. [13]
На основании данных по разбавлению рассчитывают концентрацию титана в каждой колбочке. Таким образом получают серию стандартных растворов. Далее с помощью описанного выше фотоэлектро-колориметра ( ФЭК-М) определяют оптическую плотность каждого стандартного раствора из приготовленной серии. Оптическую плотность определяют с помощью шкалы правого барабана с применением синего светофильтра. В качестве растворителя используют раствор для разбавления, состав которого указан выше. [14]
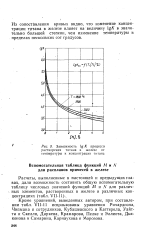 |
Зависимость lg К процесса растворения титана в железе от температуры и концентрации титана. [15] |
Страницы: 1 2 3 4