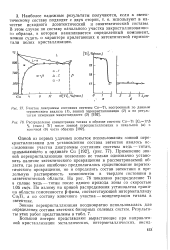
Концентрация - титан
Cтраница 3
Органическую фазу собирают в мерную пробирку емкостью 10 мл и измеряют оптическую плотность раствора, определяя концентрацию титана по калибровочному графику. Для построения калибровочного графика в делительную воронку вносят от 1 до 10 мл раствора, содержащего 1 36 мкг / мл Ti, 2 мл раствора реагента, 1 мл раствора аскорбиновой кислоты и проводят экстракцию, как описано выше. [31]
Верхняя ветвь поляризационных кривых закономерно сдвигается в область более положительных потенциалов с ростом концентрации серной кислоты при неизменной концентрации титана ( IV) в растворе. Нижняя ветвь поляризационных кривых при неизменной концентрации Ti ( S04) 2 в растворе с ростом концентрации кислоты смещаются в сторону более положительных потенциалов. [32]
Из табл. 6 следует, что Д-1 сильно зависит не только от концентрации щавелевой кислоты, но и от концентрации титана, что свидетельствует об образовании полиядерных комплексов в этих условиях [ 13, с. Вывод об образовании полиядерных комплексов не противоречит данным, полученным катионным обменом. Появление заметной окраски растворов, по-видимому, связано с образованием полиядерных форм, расчет состава и устойчивости которых оказался затруднителен. [33]
Наиболее интересной особенностью поляризационных кривых, полученных на платиновом катоде, является наличие предельного тока, величина которого увеличивается с уменьшением концентрации титана в растворе. [34]
Так же, как и при полуавтоматической дуговой сварке вольфрамовым электродом, большая доля основного металла в металле шва обусловливает уменьшение концентрации титана и снижение эффекта измельчения зерна в шве. [35]
По излому на кривой распределения установлена граница области гомогенности ( З - фазы, соответствующей интерметаллиду Cu3Ti, а по составу конечного участка - концентрация титана в эвтектике. [37]
Сохранение в структуре большого количест - sa гексагонального карбида, по-видимому, является результатом рачительного увеличения содержания хрома в стали при сравни-ельно небольшом повышении концентрации титана. Вполне воз-южно, что уменьшение содержания углерода до 1 0 - 1 2 % приво - [ ит к увеличению содержания кубического карбида. [38]
 |
Влияние легирования на константу скорости реакции k бора с титановыми сплавами. [39] |
Идеальный разбавитель должен уменьшать константу скорости реакции линейно от 5 2 - 10 - 7 см / с1 / 2 до нуля при снижении до нуля концентрации титана в сплаве; другими словами, удельная константа скорости реакции должна быть равна - 0 052 - 10 - 7 ( см / с1 / 2) / ат. С увеличением в сплаве концентрации алюминия, молибдена или ванадия скорость реакции уменьшается значительно сильнее, чем для разбавителей. Эти элементы образуют третью группу. Из анализа данных табл. 3 следует, что ванадий эффективнее тормозит реакцию взаимодействия в разбавленных растворах, чем в концентрированных. На рис. 16 показано влияние различных типов легирующих элементов на константу скорости реакции при 1033 К. Экспериментальная кривая для сплавов титан - ванадий иллюстрирует влияние концентрации на константу скорости. Из этих результатов были рассчитаны удельные константы скорости реакции, отнесенные к весовым процентам. [40]
Из рис. 5, 6, 7 видно, что поляризационные кривые на медном катоде имеют область предельных токов, величина которых растет линейно с ростом концентрации титана, почти не зависит от концентрации серной кислоты и имеет более высокие значения в перемешиваемых растворах. [41]
Измеряют 4 - 5 раз скорость реакции, находят тангенсы углов наклона прямолинейных участков кривых: время - оптиче екая плотность и строят калибровочный график в координатах концентрация титана - тангенс угла наклона. [42]
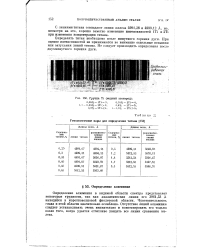 |
Группа Ti ( медный электрод. [43] |
С линиями титана совпадают линии железа 4991 28 и 4999 12 А, но, несмотря на это, хорошо заметно изменение интенсивностей ITi и 2Ti при изменении концентрации титана. [44]
Концентрация титана в растворе соответствует 20 мг / мл. [45]
Страницы: 1 2 3 4