Концентрация - фермент
Cтраница 3
Но согласно принятым обозначениям ul есть концентрация несвязанного фермента - величина, которую легко определить, так как по схеме известно, какое количество F связано в промежуточных соединениях. [31]
Напишите выражение скорости реакции с включением концентраций фермента и глюкозы, если скорость реакции пропорциональна концентрации фермента. [32]
Для олигонуклеотидов из панкреатического РНК-азного гидролизата концентрацию фермента можно снизить до 0 1 мг / мл и проводить инкубацию 30 мин при 37 С. По окончании инкубации раствор из капиллярной трубки наносят непосредственно на полоску DEAE-бумаги шириной 2 5 см и длиной 30 см. По одну сторону от гидролизата наносят образец негидролизованного олигонуклеотида, по другую - смесь розового и голубого маркеров. Полоску бумаги кладут на рамку или помещают в прибор для электрофореза и затем смачивают смесью 2 5 % - ной муравьиной кислоты и 8 7 % - ной уксусной кислоты. Этой же смесью заполняют резервуары. Электрофорез проводят при напряжении - ЗОВ / см до тех пор, пока голубой маркер не продвинется приблизительно на 1 / 3 общего расстояния. Ток отключают, бумагу осторожно вынимают и дают ей высохнуть. Положения красителей-маркеров отмечают радиоактивными чернилами и проводят радиоаутографию электрофореграммы. Измеряют расстояния пятен от старта и идентифицируют последовательность в соответствии с данными, приведенными в табл. 11.1. В сомнительном случае пятна можно элюировать и щелочным гидролизом определить нуклеотидный состав. [33]
Если концентрация субстрата во много раз больше концентрации фермента, то из условия стационарности реакции следует, что после короткого периода индукции скорость прироста фермент-субстратных комплексов становится равной скорости их убыли. [34]
Активность ферментов зависит от рН среды, концентрации фермента, температуры. [35]
Активность ферментов зависит от рН среды, концентрации фермента, температуры. Обычно наблюдается линейная зависимость. Повышение температуры приводит к увеличению активности фермента, однако при 40 - 50 С достигается ее максимум. [36]
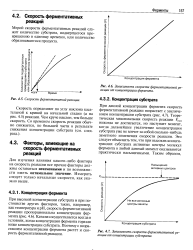 |
Зависимость скорости ферментативной реакции от концентрации фермента.| Зависимость скорости ферментативной реакции от концентрации субстрата. [37] |
Катализ осуществляется всегда в условиях, когда концентрация фермента гораздо ниже концентрации субстрата. Поэтому с возрастанием концентрации фермента растет и скорость ферментативной реакции. [38]
Начальная скорость ферментативной реакции будет прямо пропорциональна концентрации присутствующего фермента. Любое наблюдаемое отклонение от линейной зависимости вовсе не означает изменения того очевидного принципа, что две молекулы фермента вызовут превращение в результате реакции в два раза большего ( по сравнению с одной молекулой) количества вещества. Отсутствие линейной зависимости между скоростью реакции и концентрацией фермента свидетельствует о влиянии какого-то фактора, усложняющего ход реакции. Такими факторами - если мы не имеем дело со слишком быстро протекающей реакцией, в связи с чем данный метод оказывается непригодным для изучения ее кинетики, - могут быть присутствие в реакционной среде ингибитора или феномен подавления реакции ее продуктом. Обычно такое кажущееся отклонение обусловлено тем, что с помощью данного метода определения активности фермента мы на самом деле измеряем не истинную начальную скорость реакции, а лишь скорость на ранних этапах реакции. Таким образом, обнаружение нелинейной зависимости между скоростью реакции и концентрацией фермента должно прежде всего заставить исследователя критически проанализировать детали используемого метода, прежде чем пытаться строить предположения о новых принципах кинетики данной реакции. [39]
 |
График линейной трансформации ур-нии Михаэлиса - Ментен в двойных обратных величинах ( по Лайнуиверу - Берку. [40] |
При данной т-ре скорость р-ции зависит от концентраций фермента, субстрата и состава среды. Различают стационарную, предстационарную и релаксационную кинетику ферментативных р-ций. [41]
Оразных ферментативных реакций в сравнительно широком ряду концентраций ферментов. [43]
Какие бы средства ни использовались для изменения концентраций уже имеющихся ферментов, возможности количественной стратегии в компенсации температурных эффектов весьма значительны. Увеличение концентрации ферментов при низких температурах и уменьшение при высоких температурах могли бы существенно стабилизировать интенсивность обмена - особенно если речь идет о ферментах, лимитирующих скорость какого-либо процесса. [44]
Если повысить концентрацию субстрата, сохраняя постоянной концентрацию фермента, то скорость возрастает пропорционально концентрации субстрата; но если увеличивать все больше и больше концентрацию субстрата, то настанет такой момент, когда скорость не будет меняться с ростом концентрации субстрата. Действительно, когда все активные центры фермента заняты, дальнейшее повышение концентрации S в растворе не приводит к увеличению скорости реакции. [45]
Страницы: 1 2 3 4
