Концентрация - фермент
Cтраница 4
При избытке концентрации лиганда по сравнению с концентрацией фермента ( именно в этих условиях обычно и йротекают ферментативные реакции; см. гл. [46]
Скорость ферментативной реакции находится в определенной зависимости от концентрации фермента и является мерой каталитического действия последнего. Она часто называется активностью и выражается в стандартных единицах. Комиссией по ферментам Международного биохимического союза за единицу количества фермента, обозначаемую символом Е, предложено принимать такое количество его, которое превращает 1 мкмоль субстрата или 1 мкэквивалент реагирующей группы или разрываемой связи в 1 мин при стандартных условиях. [47]
Скорость реакции, катализируемой ферментом, прямо пропорциональна концентрации фермента. При низкой концентрации субстрата реакция имеет первый порядок по субстрату. Скорость реакции зависит от температуры и кислотности среды. [48]
 |
Схематическое представление процесса концентрирования реагирующих молекул А и В из разбавленного раствора на активном центре фермента. [49] |
Это связано в основном с тем, что концентрация фермента и соответственно активных центров в растворе является, как правило, столь малой, что локальное увеличение концентрации реагентов не может привести к очень большому увеличению суммарной скорости реакции. [50]
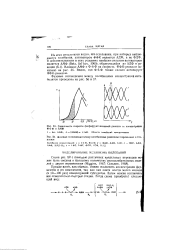 |
Зависимость скорости фосфофруктоки казной реакции от концентрации Ф - б - Ф и АМФ. [51] |
Прежде всего, как обычно, можно исключить концентрации ферментов и их комплексов, так как они почти всегда много меньше ( в 10 - 100 раз) концентраций субстратов. [52]
Хотя эктотермные эукариоты обладают двумя главными механизмами увеличения концентраций ферментов при адаптации к холоду или уменьшения их при адаптации к теплу, важно уяснить себе, что эти два механизма неравноценны по своим возможностям. Скорость расщепления может влиять только на количества тех ферментов, которые уже есть в клетке, тогда как синтез ( связанный с транскрипцией и трансляцией новой генетической информации) может вести к появлению новых разновидностей ферментов - обстоятельство, к которому мы еще вернемся. [53]
Уравнение (6.16) описывает экспериментально наблюдаемую зависимость скорости реакции от концентрации фермента, кислорода, ионов водорода. [54]
При постоянной концентрации альдегида и нитрата превращение прямо пропорционально концентрации фермента в ранних стадиях восстановительного процесса; в более поздних стадиях наблюдаются незначительные отклонения от этой закономерности. [55]
При условии избытка субстрата скорость ферментативной реакции зависит от концентрации фермента. Эта зависимость подчиняется уравнению прямой: У k - [ E ], где [ Е ] - концентрация фермента. [56]
Начальная скорость ферментативной реакции при условии избытка субстрата пропорциональна концентрации фермента: vkE, где k - константа скорости реакции; Е - концентрация фермента. При графическом изображении этой зависимости получается прямая линия. [57]
Оптимальное значение рН должно быть определено при выбранных значениях концентрации фермента и насыщающей концентрации субстрата, температуре ( 37 0 1) С и использовании буферного раствора того состава, который не ингибирует фермент. [58]
Уравнение ( 2) выражает зависимость скорости ферментативной реакция от концентрации фермента и субстрата. [59]
Страницы: 1 2 3 4