Концентрация - форма
Cтраница 3
Уравнение (8.12) связывает кинетический ток ik с площадью электрода, константой скорости образования формы Ох из А, концентрацией формы А на поверхности электрода и толщиной реакционного слоя. [31]
Однако нетрудно видеть, что R и Л / а не являются константами, так как они зависят от концентраций обменивающихся форм. [32]
Как видно из рис. 211, при удалении уровня Ферми от валентной зоны и приближению его к зоне проводимости увеличивается концентрация акцепторной формы и падает содержание донорной. При этом концентрация слабой формы проходит через максимум. Напротив когда уровень Е значительно выше V, то главная масса хемад-сорбированных частиц существует в акцепторной форме ( - 1Х Сказанное обусловлено тем, что положением уровня Ферми определяется концентрация свободных электронов и их вакансий на поверхности кристалла. [33]
Окраска индикатора при переходе одной формы в другу заметна тогда, когда после прибавления любого окислителя ш восстановителя установится соотношение концентраций форм индикатора окисленной и восстановленной в 10 раз больше ш меньше. [34]
Если в воде имеются ионы, которые вступают в реакцию с продуктами диссоциации растворенных газов, то это должно повысить концентрацию диссоциированных форм растворенного газа. [35]
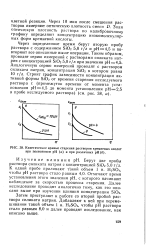 |
Кинетические кривые старения растворов кремневых кислот при постоянном рН ( а и при различных рН ( б. [36] |
Через 10 мин после смешения растворов измеряют оптическую плотность смеси D, Зная оптическую плотность раствора по калибровочному графику определяют концентрацию низкомолекулярных форм кремневой кислоты. [37]
Окраска индикатора при переходе одной формы в другую заметна тогда, когда после прибавления любого окислителя или восстановителя, установится соотношение концентраций формы индикатора окисленной и восстановленной в 10 раз больше или меньше. [38]
При больших значениях плотности тока обмена зависимость потенциала электрода от времени, наблюдаемая при включении поляризующего тока постоянной плотности, определяется изменением концентрации реагирующих форм у поверхности электрода. При электровосстановлении сульфатных комплексов кадмия на кадмиевом электроде из растворов с концентрацией ионов кадмия 10 - 3М и плотностях тока порядка 10 - 4 - 10 - 3 А-см - 2 равновесие электродной реакции практически не нарушается, и изменение потенциала кадмиевого катода определяется закономерностями нестационарной диффузии ионов кадмия ( II) к поверхности электрода. Когда концентрация ионов кадмия у поверхности электрода уменьшится практически до нуля, потенциал электрода начинает быстро смещаться до значений, при которых выделяется водород. Выделение водорода в области потенциалов хронопотенциометрической волны восстановления кадмия ( II) практически не происходит в связи с большой величиной перенапряжения водорода на кадмии. [39]
Подтверждением данного микродеформационного механизма наводороживания в вершине трещины является повышенная на 2 - 3 порядка плотность дислокаций под КРН изломом и превышающая норму концентрация низкотемпературных микродеформационных форм водорода, отсутствующих в металлургическом фоне. Наводороживание не подверженных растрескиванию объемов трубы не обнаружено. [40]
Если реагирует нейтральная молекула, то наклон прямой значительно меньше, так как рост активности ионов D по мере роста кислотности среды компенсируется падением концентрации непро-тонированной формы. [41]
Чалая экстрагировали бесцветную форму родамина С бензолом и эфиром из растворов со значениями рН, равными 5 и 1, и определили равновесные соотношения концентраций бесцветной формы в экстракте и окрашенной в водной фазе. [42]
Отношение летучести компонента в газовой фазе к суммарной концентрации растворенного вещества во всех формах может приближаться к нулю с увеличением разведения раствора из-за того, что концентрация диссоциированных форм становится бесконечно больше концентрации недиссоциированной формы. [43]
Следует отметить, что в CH3CN относительная интенсивность полосы при 1021 см - выше, чем в СН2С12; это свидетельствует о том, что в CH3CN концентрация формы 2 больше. [44]
Таким образом, на примере сорбции ЭДТА и ДТПА показано, что сорбция полиаминополикарбоксильных кислот описывается уравнениями, вытекающими из уравнения закона действующих масс, если учитывать концентрацию сорбируемой формы в растворе. Сопоставление констант сорбции, а также теплот сорбции ЭДТА и ДТПА показывает, что при сорбции этих аминокислот сульфокатионитом существенную роль играет взаимодействие углеводородных цепей сорбированных молекул с каркасом полимера, а также и межмолекулярные взаимодействия сорбированных аминокислот. [45]
Страницы: 1 2 3 4