Концентрация - хемосорбент
Cтраница 3
Равновесное давление компонента на границе раздела фаз учи-тывает влияние свойств жидкой фазы и происходящих в ней процессов на скорость абсорбции и является функцией концентрации свободных молекул абсорбтива на границе раздела фаз. Последняя при прочих равных условиях уменьшается при увеличении концентрации хемосорбента, константы скорости химической реакции ж коэффициента диффузии молекул активной части хемосорбента. Противоположное влияние наблюдается при увеличении коэффициента диффузии самих молекул абсорбтива. [31]
Выражение (6.87) записано при условии, что валентности реагирующих компонентов равны между собой. Если валентности экстрагента и хемосорбента не равны, то концентрацию хемосорбента следует умножить на стехиометрический коэффициент. [32]
А при выполнении условия М 1 усиливается зависимость К / от концентрации хемосорбента: величина п в зависимости Kr-BiKni возрастает и становится равной двум. Поэтому можно также сделать вывод, что повышение давления и концентрации хемосорбента является более мощным средством интенсификации хемосорбционных процессов, проводимых в аппаратах пленочного типа, по сравнению с процессами, проводимыми в аппаратах барботажного типа. [33]
Процессы хемосорбции анализируются при реакциях типа х те - с методами численного интегрирования. Результаты подобных расчетов указывают на своеобразную особенность в характере изменения концентрации хемосорбента по толщине диффузионной пленки; в условиях избытка активной части раствора практически всегда наблюдается линейный закип ее изменения от некоторого значения Вр на границе раздела до Вж в основной массе жидкости. [34]
 |
Влияние концентрации реагентов Аж, Еж, Рж на коэффициент ускорения массопередачи f при а ( 1. [35] |
Следует отметить противоречивость различных рекомендаций по расчету ч для массопередачи с необратимой реакцией нулевого порядка по хемосорбенту. Бриана [50] обнаруживается зависимость v от М и, следовательно, от концентрации хемосорбента. Вопрос о расчете кинетики массопередачи с реакцией нулевого порядка по В требует дополнительного исследования. [36]
При указанных условиях ( R5 М, Вжбжкрит) процесс лимитируется диффузией в газовой фазе. Чем выше парциальное давление передаваемого компонента в газе, тем выше Вж крит и, следовательно, тем выше надо иметь концентрацию хемосорбента, чтобы перевести сопротивление в газовую фазу. [37]
Так, применительно к процессу разделения технологического газа в производстве аммиака показано [238], что габариты абсорбера, поверхность теплообменной аппаратуры уменьшаются, если повысить температуру жидкости. Данные, приведенные на рис. 7.1, получены на основе метода локальной оптимизации при определенных ограничениях ( постоянная производительность по газу в жидкости, концентрация хемосорбента, давление и др.); зависимость степени извлечения СС2 от температуры получена численным методом на основе моделирующего алгоритма по программе ABS ( см. разд. [38]
По механизму поглощения, согласно имеющейся классификации [3], рассматриваемая система представляет собой случай абсорбции с необратимой химической реакцией в жидкой фазе. Ими было установлено, что при низких концентрациях двуокиси углерода в газовой фазе скорость поглощения прямо пропорциональна парциальному давлению двуокиси углерода и не зависит от концентрации хемосорбента в растворе. [39]
Это означает, что в предельных гидродинамических режимах величина коэффициента селективности К одинакова. Если же для одного из компонентов существенную роль играет сопротивление в газовой фазе, то, как видно из уравнений (5.44) и (5.45), величина К зависит от концентрации хемосорбента и, следовательно, от степени перемешивания жидкости. [40]
Например, в работе [193] получено численное решение системы уравнений (5.8) и (5.9) при следующих условиях: 1) движение газа можно рассматривать как поршневой поток; 2) сопротивление в газовой фазе ничтожно мало; 3) порядок реакции по передаваемому компоненту А произволен, но концентрация хемосорбента велика по сравнению с А. Полученные решения использованы для анализа работы колонных барботажных реакторов. Те же допущения положены в основу работы [189], но рассмотрена и область протекания мгновенной реакции. [41]
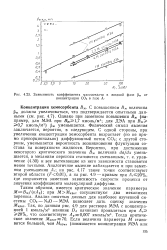 |
Зависимость коэффициента массоотдачи в жидкой фазе концентрации СО2 в газе Лг. [42] |
Однако при заметном повышении Вж ( например, для МЭА при В ] ж 1 7 кмоль / м3; для ДЭА при В ж 0 7 кмоль / м3) рж уменьшается. Физический смысл явления заключается, вероятно, в следующем. С одной стороны, при увеличении концентрации хемосорбента возрастает ( но не прямо пропорционально) диффузионный поток СО2; с другой стороны, уменьшается вероятность возникновения флуктуации состава на поверхности жидкости. Аналогичное явление наблюдается и при заметном уменьшении Лг; на рис. 4.17 такие точки соответствуют второй области ( / г0 01), а на рис. 4.9 - кривым при Лг 20 %, где сохраняется заметная зависимость скорости процесса от значения коэффициента молекулярной диффузии. [43]
Пусть растворенный в капле экстрагент, диффундируя в сплошную фазу, вступает там в химическую реакцию второго порядка с хемосорбентом. Будем считать, что вдали от частицы концентрация хемосорбента постоянна по объему и что в течение всего процесса поток хемосорбента через поверхность капли отсутствует. [44]
Исследованию и расчету колонных химических реакторов и процессам абсорбции и десорбции в колонных аппаратах посвящена обширная литература. Большинство работ относится к экспериментальному изучению конкретных систем и получению эмпирических формул для расчета аппаратов. В ряде работ применяются пленочная и пенетра-ционная модели массопередачи с химическими реакциями, изложенные в гл. Поскольку, однако, эти модели разработаны для случая постоянства концентрации хемосорбента и абсорбтива ( экстрактива) в сплошной и дисперсной фазах, их применение для расчета прямо - и противоточных аппаратов затруднено. Обычно при расчете колонных аппаратов полагают, что коэффициент ускорения массообмена вследствие протекания химических реакций постоянен по высоте колонны. Это допущение может привести в ряде случаев к существенным ошибкам. [45]
Страницы: 1 2 3