Концентрация - хлор-ион
Cтраница 2
Такое различие в концентрации хлор-ионов оказывает влияние и на скорость коррозии. [16]
Потенциал зависит от концентрации хлор-ионов. Такие электроды называются электродами второго рода. [17]
Скорость абсорбции будет пропорциональна концентрации хлор-ионов в жидкости; отсюда предельная скорость, при которой золото еще может растворяться ( соответственно - предельная плотность тока), будет пропорциональна концентрации хлор-ионов. Если плотность тока повышается, процесс абсорбции хлор-ионов не может итти с той же скоростью, что и коррозия, и гидроксильные ионы начинают играть роль в анодной реакции, ведя к образованию пленки окиси ( или гидроокиси) на поверхности и, следовательно, к пассивности. Значение рН ( 10 8 в 1 N растворе хлористого калия), выше которого tp внезапно падает, соответствует условиям, при которых прямая абсорбция ОН - ионов может соревноваться с абсорбцией СГ-ионов, сильно облегчая таким образом наступление пассивности. [18]
Таким образом, увеличение концентрации хлор-иона в растворе путем введения определенных количеств хлористого аммония ведет к наиболее полному переходу их в соединения типа указанного комплекса, а следовательно, и к уменьшению возможности образования галлатов. Экспериментальные данные подтвердили эти выводы, и на основании их нами был выработан следующий метод работы. [19]
Наиболее подходящим для определения концентрации хлор-ионов является фотоколориметрический дифенилкарбазидный метод. Этот метод может быть использован как визуальный, но лишь для периодического контроля, так как для визуального определения требуется частое приготовление свежей шкалы. [20]
В насыщенном растворе постоянство концентрации хлор-ионов поддерживается автоматически. Однако недостатком такого электрода является большой температурный коэффициент, вызванный изменением концентрации насыщенного раствора хлорида калия при изменении температуры. [21]
 |
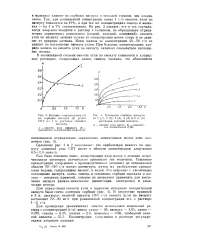
Зависимость адсорбции хлор-ионов на поверхности стали 12Х18Н10Т от концентрации NaCl и длительности выдержки ( цифры у кривых при потенциале коррозии данные Герасимова В. В. и др. ]. [22] |
Подкисление среды и увеличение концентрации хлор-иона меняет электрохимическую ситуацию. [23]
 |
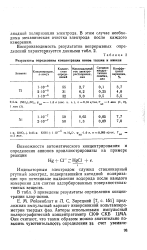
Влияние хлорида олова ( 1 на сорбцию штсмута ( 2 углем СКТ и г. 1 м. раствора соляной.| Изотермы сорбции висмута. [24] |
Как было отмечено выше, концентрация хлор-ионов в реально встречающихся растворах значительно превышает эти величины. [25]
Потенциал нулевого заряда зависит от концентрации хлор-иона. [26]
Оказалось, что при увеличении концентрации хлор-ионов от 0 002 до 0 02 М скорость реакции заметно не менялась. [27]
Ниже приведены результаты исследования влияния концентрации хлор-ионов на анодное поведение сталей 18 Сг-14 Ni, а также сталей на этой основе, дополнительно легированных 2 5 % V, Si, Mo или Re, в кислых и нейтральных средах. [28]
Книбс и Палфримен22 нашли, что концентрация хлор-ионов устанавливается на постоянном уровне и зависит от температуры. [29]
 |
Результаты определения концентрации ионов таллия и никеля. [30] |
Страницы: 1 2 3 4