Концентрация - хлорид-ион
Cтраница 3
Выход винилацетата существенно зависит от концентрации хлорид-иона. [31]
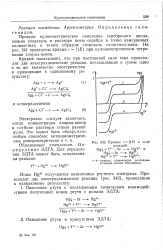 |
Кривые i f ( E в ходе. [32] |
Электролиз следует закончить, когда концентрация хлорид-ионов в глубине раствора станет равной нулю. [33]
Потенциал этого полуэлемента зависит от концентрации хлорид-ионов X, и она должна быть фиксированной для каждого электрода. [34]
 |
Кривые титрования 50 00 мл. [35] |
Дальнейшее добавление нитрата серебра понижает концентрацию хлорид-ионов, и кривая превращается в кривую, характерную для титрования одного хлорида. [36]
В настоящее ареия измеррцяе относительно больших концентрация хлорид-иона не представляет трудностей, т.к. существует методы [ 10 ], позволявшие контролировать концентрацию хлорид-иона с достаточной точ-ностьо и надежностьо. [37]
Очевидно, эти равновесия зависят от концентрации хлорид-ионов в растворе. Изменяя концентрацию этих ионов, можно осуществить ряд интересных разделений. [38]
 |
Схема определения стандартного электродного потенциала системы. [39] |
Электродный потенциал этой системы зависит от концентрации хлорид-ионов. [40]
Очевидно, эти равновесия зависят от концентрации хлорид-ионов в растворе. Изменяя концентрацию этих ионов, можно осуществить ряд интересных разделений. [41]
Данная реакция обратима, и повышение концентрации хлорид-ионов смещает ее равновесие вправо. В результате раствор обесцвечивается. [42]
Для приготовления рабочего контрольного раствора с концентрацией хлорид-иона 50 мкг / л берут пипеткоа 50 мл исходного контрольного раствора Э в нервуо колбу вместимостьв 500 ил, добавляет 5 мл O. IH азотное кяелоты и доводят обеохлореннои водов до метки, при этом рН раствора получает равным 3 0 единицам. [43]
Интересно, что при тех же концентрациях хлорид-ионов в водной фазе гидратные числа 1лТ1С14 для всех растворителей меньше гидратных чисел НТ1С14 ( сравн. Это можно объяснить более сильной гидратацией гидроксо-ния, в котором положительный заряд не распределен по поверхности, а концентрируется на атомах водорода. Молекулы воды в структуре гидратированного гидроксония в результате миграции положительного заряда могут временно становиться гидроксонием и поэтому образовывать сильную водородную связь с другими молекулами воды и с органическим растворителем. Гидратация же иона лития сводится, в общем, к взаимодействию с ближайшими молекулами воды. [44]
Результаты изучения экстракции цинка в зависимости от концентрации хлорид-ионов использованы нами для определения состава хлоридных комплексов цинка. Используемый обычно для расчета состава комплексов метод сдвига равновесия [1], как известно, не дает возможности определить общее количество аддендов в комплексе. По этому методу рассчитывается лишь число п аддендов, присоединяющихся на данной ступени комплексообразования. [45]
Страницы: 1 2 3 4