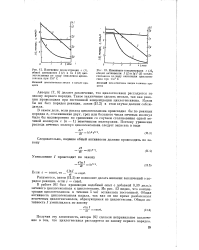
Концентрация - циклогексанол
Cтраница 1
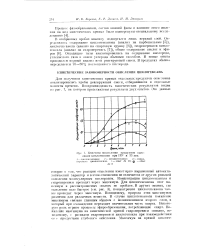 |
Кинетика накопления продуктов окисления циклогексана при 135 и 33 атм. [1] |
Концентрации циклогексанола и гидроперекиси проходят через максимум. Для циклогексанона этот максимум в рассматриваемых опытах не пройден. В других опытах, где окисление шло быстрее ( см. рис. 3), концентрация циклогексанона также проходит через максимум. Невидимому, природа этих максимумов различна для различных веществ. В случае циклогексанола появление максимума связано главным образом с возникновением второго слоя, в который при охлаждении переходит значительная часть спирта. Некоторую роль играют процессы эфирообразования, потребляющие спирт. Появление максимума на кинетической: кривой гидроперекиси связано, по-видимому, с распадом гидроперекиси циклогексила при взаимодействии ее с продуктами глубокого окисления. [2]
В ходе реакции концентрация циклогексанола, как правило, соизмерима с концентрацией циклогексанона. Кроме этого соединения, других одноатоМ - ных спиртов при окислении циклогексана в заметных количествах не образуется. При выделении 3 5-динитробензоатов из продуктов окисления циклогексана эфир циклогексанола может быть выделен с выходом 93 1 мол. Учитывая неизбежные потери при выделении, можно считать, что среди спиртовых продуктов циклогексанола содержится не менее 95 мол. [3]
Разбавляют раствор А до концентрации циклогексанола 0 015 мг / мл. [4]
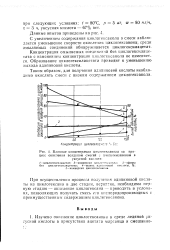 |
Влияние концентрации цихлотексанола на процесс окисления воздухом смесей с цчклогеисаноном в. [5] |
Концентрация омыляемых соединений без циклогексилаце-тата с изменением концентрации циклогексанола не изменяется. Образование циклогексилацетата приводит к уменьшению выхода адипиновой кислоты. [6]
По этим данным можно определить, что при изменении концентрации циклогексанола на 13 % ( смесь № 5) чувствительность будет равна 15 %, а при 20 % ( смесь № 6) 6t) 23 % при длине кюветы, равной 4 мм. [7]
Приведенные положения хорошо согласуются с результатами эксперимента. Действительно, с повышением температуры возрастает концентрация циклогексанола и монокарбо-новых кислот - продуктов мономолекулярного превращения и падает содержание адипиновой кислоты. Циклогексанон, как следует из нашей предыдущей работы, образуется при цепном распаде гидроперекиси, энергия активации его ниже, чем для мономолекулярного процесса, поэтому содержание кето-на мало меняется с ростом температуры. [8]
В работе [6] был произведен подобный опыт с добавкой 0 39 моль / л меченого циклогексанола к циклогексану. Из рис. 13 видно, что концентрация циклогексанола в течение 5 час оставалась постоянной. Общая активность циклогексанола падала, так как он все время разбавлялся немеченым циклогексанолом, образующимся из циклогексана. [10]
Циклогексилнитрит экстрагируют каким-либо углеводородом и на спектрофотометре СФ-4 при длине волны 345 / ир, определяют оптическую плотность раствора. По величине этой плотности и графику оптическая плотность - концентрация циклогексанола определяется концентрация циклогексанола в пробе. [11]
Циклогексилнитрит экстрагируют каким-либо углеводородом и на спектрофотометре СФ-4 при длине волны 345 / ир, определяют оптическую плотность раствора. По величине этой плотности и графику оптическая плотность - концентрация циклогексанола определяется концентрация циклогексанола в пробе. [12]
ПАВ в водно-спиртовых смесях почти одинакова. Область расслаивания, примыкающая к стороне треугольника вода - смесь органических спиртов, увеличивается с повышением концентрации циклогексанола в смеси спиртов. [13]
Другой метод повышения выхода кетона и спирта сводится к прекращению реакции на стадии образования гидроперекиси циклогексила. В обычных условиях окисления ( стальной реактор, использование солевых катализаторов) концентрация гидроперекиси мала и увеличивается практически параллельно с увеличением концентраций циклогексанола и циклогексанона. Это связано с повышенной скоростью распада, и в этих условиях трудно рассчитывать на получение существенного выигрыша. [14]
Изучены разрезы четырехкомпонентной системы синтанол ДС-10 - смесь органических спиртов - вода, причем количество циклогексанола и изопропилового спирта соотносятся как 20: 80, 40: 60, 60: 40 и 80: 20 % мае. Область гетерогенных смесей располагается на диаграммах растворимости разрезов узкой полосой вдоль стороны ПАВ - смесь органических спиртов, с увеличением в смеси содержания циклогексанола гетерогенная область несколько уменьшается. Область расслаивания появляется на треугольниках состава при концентрации циклогексанола в смеси органических спиртов 40, 60 и 80 % мае; при повышении концентрации циклогексанола в смеси область расслаивания увеличивается. [15]
Страницы: 1 2