Концентрация - свободная щелочь
Cтраница 3
Сероуглерод, выделяющийся при частичном омылении ксантогената, реагирует со щелочью или сернистым натрием, находящимся в растворе, с образованием сернистых и полисернистых соединений. Поэтому, наряду с понижением степени этерифика-ции ксантогената целлюлозы, в процессе созревания увеличивается количество сернистых соединений и уменьшается концентрация свободной щелочи в растворе. [31]
Сероуглерод, выделяющийся при частичном омылении ксантогената, реагирует со щелочью или сернистым натрием, находящимся в растворе, с образованием сернистых и полисернистых соединений. Поэтому, наряду с понижением степени эге-рификашш ксантогената целлюлозы, в процессе созревания увеличивается количество сернистых соединений и уменьшается концентрация свободной щелочи в растворе. [32]
Для проверки щелочного раствора гипохлорита калия применяют следующий очень простой способ. KJ; после растворения иодида туда приливают точно отмеренные ( специально прокалиброванной пипеткой) 2 мл раствора гипохлорита калия. Концентрация свободной щелочи в растворе гипохлорита и его нормальность по гипохлориту) определяются расчетом, основы которого ясны из следующего. [33]
 |
Установка для приготовления раствора гипохлорита. [34] |
Проверку щелочности раствора гипохлорита производят следующим образом. KJ; после растворения иодида туда приливают точно отмеренные ( специально откалиброванной пипеткой) 2 см3 раствора гипохлорита. Концентрация свободной щелочи в растворе гипохлорита определяется расчетом, основы которого видны из следующего. [35]
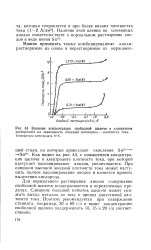 |
Влияние концентрации свободной щелочи в станнатном электролите на зависимость анодный потенциал - плотность тока. Температура электролита 70 С. [36] |
Для нормального растворения анодов содержание свободной щелочи поддерживается в определенных пределах. Слишком большой избыток щелочи может снижать выход металла по току и предел допустимой плотности тока. Поэтому рекомендуется при содержании станната, например, 30 и 60 г / л и выше концентрацию свободной щелочи поддерживать 10, 15 и 20 г / л соответственно. [37]
Величина катодной плотности тока в сильной степени зависит от концентрации в растворе свободного цианида и едкой щелочи. Из приведенных выше уравнений следует, что с повышением концентрации NaCN - или KCN, а также NaOH или КОН концентрация ионов цияка Zn2 в растворе понижается, а следовательно, растет катодная поляризация. Концентрация свободного цианида не должна быть слишком высокой, чтобы избежать значительного снижения катодного выхода по току, но достаточной для обеспечения устойчивости электролита и предотвращения условий, вызывающих пассивирование анодов. Аналогичные требования относятся и к концентрации свободной щелочи в электролите. [38]
Известно, что скорость гидролиза сложноэфирной связи в водном растворе щелочного агента с повышением температуры значительно возрастает. Однако установлено [176], что она зависит от концентрации щелочного агента и, если последняя не превышает 3 - 4 % ( масс.), то даже при температуре выше 100 С степень гидролиза эфира при нейтрализации невелика. Вначале эфир-сырец смешивают с водным раствором щелочного агента при 60 - 80 С. При смешении нейтрализация завершается на 70 - 80 % и концентрация свободной щелочи в реакционной массе резко падает. Далее образующуюся дисперсную систему нагревают до температуры кипения водного раствора щелочи и нейтрализация завершается при непрерывной гетероазеотропной отгонке водно-спиртовой паровой смеси. Пары воды и спирта, образующиеся при кипении, конденсируются и охлаждаются в холодильнике. Конденсат расслаивается во флорентийском сосуде на спирт и воду. Вода непрерывно возвращается в нейтрализатор, а спирт отделяется для последующего использования на стадии этерификации. [39]
В простых кислых растворах потенциал меди положитель-нее потенциала олова примерно на 0 5 В, поэтому для совместного осаждения этих металлов пользуются растворами их комплексных солей, цианида меди и станната калия или натрия. Стационарные и катодные потенциалы меди и олова в этих растворах довольно близки и поэтому изменение относительного содержания металлов в растворе заметно отражается на составе сплава. Однако наибольшее влияние на состав сплава оказывает концентрация свободного цианида и свободной щелочи. С повышением концентрации свободного цианида в растворе увеличивается содержание олова в осадке, с повышением концентрации свободной щелочи, наоборот, содержание олова уменьшается, а меди увеличивается. [40]
В простых кислых растворах потенциал меди положительнее потенциала олова примерно на 0 5 В, поэтому для совместного осаждения этих металлов пользуются растворами их комплексных солей, цианида меди и станната натрия или калия. Стационарные и катодные потенциалы меди и олова в этих растворах довольно близки, и потому изменение относительного содержания металлов в растворе заметно отражается на составе сплава. Однако наибольшее влияние на состав сплава оказывает концентрация свободного цианида и свободной щелочи. С повышением концентрации свободного цианида в растворе увеличивается содержание олова в осадке, с повышением концентрации свободной щелочи - наоборот, содержание олова уменьшается, а меди увеличивается. Это объясняется влиянием цианида и щелочи на катодные - потенциалы выделения меди и олова из цианисто-стан-натного электролита. [41]
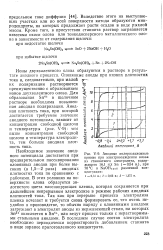 |
Анодные поляризационные кривые при электроосаждении олова из станнатного электролита, содержащего 16 1 г / л Sn ( - 0 54 н., при. [42] |
Ионы двухвалентного олова образуются в растворе в результате анодного процесса. Оловянные аноды при низких плотностях тока и, следовательно, при малой их поляризации растворяются S преимущественно с образованием j ионов двухвалентного олова. Для образования Sn 4 - в щелочном с растворе необходима повышен - ная анодная поляризация. Анод - w ная плотность тока, при которой Е достигается требуемое значение анодного потенциала, зависит от концентрации свободной щелочи и температуры ( рис. V-9): чем выше концентрация свободной щелочи и температура электролита, тем больше анодная плотность тока. [43]
Было установлено, что равновесная концентрация SiO2 в этих условиях мало зависит от начальной концентрации соды и в разных растворах имеет примерно одинаковое значение - около 7 г / л при 350 С и давлении 35 МПа. На основании этого можно было бы предполагать, что скорость роста кварца не должна зависеть от начальной концентрации содового раствора. Опыт, однако, показывает, что состав растворов в условиях роста мало отличается по содержанию SiO2, но существенно отличается по концентрации свободной щелочи. Определение щелочности отработанных растворов показывает, что чем выше концентрация соды в исходном растворе, тем выше концентрация свободной щелочи в условиях роста, несмотря на осаждение сравнительно большого количества тяжелой фазы. Это, вероятно, объясняется тем, что при сравнительно быстром нагревании автоклава во время ввода его в заданный режим равновесное состояние между реагентами не достигается, что приводит к более высокой остаточной концентрации соды. Более высокая остаточная концентрация свободной щелочи, безусловно, должна оказывать влияние на величину рН раствора, а это, в свою очередь, должно влиять на скорость роста кристаллов. [44]
Было установлено, что равновесная концентрация SiOz в этих условиях мало зависит от начальной концентрации соды и в разных растворах имеет примерно одинаковое значение - около 7 г / л при 350 С и давлении 35 МПа. На основании этого можно было бы предполагать, что скорость роста кварца не должна зависеть от начальной концентрации содового раствора. Опыт, однако, показывает, что состав растворов в условиях роста мало отличается по содержанию SiO2, но существенно отличается по концентрации свободной щелочи. Определение щелочности отработанных растворов показывает, что чем выше концентрация соды в исходном растворе, тем выше концентрация свободной щелочи в условиях роста, несмотря на осаждение сравнительно большого количества тяжелой фазы. Это, вероятно, объясняется тем, что при сравнительно быстром нагревании автоклава во время ввода его в заданный режим равновесное состояние между реагентами не достигается, что приводит к более высокой остаточной концентрации соды. Более высокая остаточная концентрация свободной щелочи, безусловно, должна оказывать влияние на величину рН раствора, а это, в свою очередь, должно влиять на скорость роста кристаллов. [45]
Страницы: 1 2 3 4