Малая концентрация - ингибитор
Cтраница 1
Малые концентрации ингибитора, хотя и смещают потенциал в положительную сторону, однако не оказывают существенного влияния на анодную поляризуемость стали. Это подтверждает вывод, сделанный при изучении этого же вопроса методом химической пассивации, о преимущественном влиянии малых концентраций ингибитора на эффективность катодного процесса. [2]
При малой концентрации ингибитора в растворе из-за сравнительно медленной подачи ингибитора к поверхности электрода и выравнивания его концентрации в приэлектродном слое по сравнению с ее величиной в объеме раствора общая скорость электродного процесса является сложной функцией времени. Так как приэлектродная ( объемная) концентрация ингибитора вследствие выравнивания его концентраций непрерывно повышается со временем жизни капли, то общая константа скорости электродного процесса, как показал Кастенинг [100], постепенно уменьшается. [3]
 |
Зависимость истинной скорости коррозии стали от концентрации силиката натрия в 0 1 н. Na2SO i. [4] |
При малых концентрациях ингибитора скорость коррозии возрастает. Более высокие концентрации защищают сталь полностью. Оказалось, что концентрации силиката ( от 10 до 100 мг / л), являющиеся эффективными для защиты от коррозии в проточных системах, не уменьшают в заметной степени коррозию в замкнутых системах с покоящимся объемом электролита. Для эффективной защиты таких систем требуются значительно более высокие концентрации силиката. Малые концентрации силиката обычно приводят к увеличению скорости коррозии. Однако эта коррозия отличается от наблюдаемой в присутствии малых концентраций хроматов и нитритов: она носит менее выраженный локальный характер, вместо питтингов и язв появляются местные очаги коррозии, занимающие относительно большую площадь. Такой вид местной коррозии, по сравнению с язвенной, является менее опасным, и в этом отношении силикаты обладают преимуществами перед хромата-ми и нитритом натрия. [5]
При малых концентрациях ингибитора в воздухе горение продолжается, но идет только до окиси углерода; при больших концентрациях ингибитора горение полностью прекращается, несмотря на высокое содержание кислорода в газовой смеси. [6]
При малых концентрациях ингибитора z стремится к нулю и Хх - 1; характер изменения q с уменьшением X не ясен. [7]
При малых концентрациях ингибитора z стремится к нулю и Хх - 1; характер изменения с уменьшением X не ясен. [8]
Кривая имеет характерный максимум в области малых концентраций ингибитора, следовательно, неполная защита железа от коррозии с помощью нитрита натрия опасна. Полной защиты можно достигнуть, применяя концентрации, которым соответствуют ничтожно малые скорости коррозии. [9]
 |
Зависимость плотности тока коррозии стали от потенциала, который задается электроду с помощью NaV03 и Na3V04 Fa - площадь активной части. [10] |
Ортованадат Na3V04 изменяет скорость анодной реакции по-другому: малые концентрации ингибитора ( до 2 г / л) не изменяют активную часть поверхности; потенциал при этом также слабо меняется, в результате чего скорость коррозии не претерпевает существенных изменений. В результате увеличивается эффективность катодного процесса и потенциал электрода смещается в положительную сторону. Когда потенциал электрода достигает примерно - 0 175 В, начинается активное воздействие ингибитора на анодную реакцию и скорость растворения падает. При потенциале - 0 2 В электрод переходит в пассивное состояние. Таким образом, механизм защиты и поведение электрода при неполной защите определяются различиями в строении анионов VO. При этом метаванадат натрия является единственным известным анодным ингибитором, который не способен усиливать коррозию при неполной защите. [11]
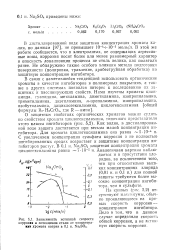 |
Зависимость истинной скорости. [12] |
Как видно, в дистиллированной воде защита достигается при весьма малой концентрации ингибитора. Для хромата циклогексиламина она равна - 5 - 10 - 4 и. С увеличением концентрации сульфата коррозия в не полностью ингибированных средах возрастает и защитные концентрации ингибиторов растут. [13]
 |
Влияние нитрита натрия на. [14] |
Электродный потенциал стали с изменением концентрации ингибитора меняется следующим образом: малые концентрации ингибитора слабо изменяют значение потенциала; при - 5 - 10 - 2 моль / л отмечается резкое смещение потенциала в положительную сторону, которое сопровождается увеличением истинной скорости коррозии. Дальнейшее увеличение концентрации ингибитора вызывает сдвиг потенциала в положительную сторону, однако не такой сильный, как малые и средние концентрации. [15]
Страницы: 1 2 3
