Начальная концентрация - гидроперекись
Cтраница 1
Начальная концентрация гидроперекиси не влияет на каталитическую константу скорости, что свидетельствует об отсутствии индукционного разложения гидроперекиси. Стеарат цинка не обладает каталитической активностью. [1]
Если начальная концентрация гидроперекиси была невысокой ( не выше 0 1 мол / л), то во всех растворителях ( за исключением к-нонана) реакция имела первый порядок. Эта закономерность сохранялась до 75 - 85 % падения начальной концентрации гидроперекиси, после чего наблюдалось заметное торможение реакции. [2]
С ростом начальной концентрации гидроперекиси кумола в ее смеси с кумолом сильно повышается скорость ее разложения, а следовательно, увеличивается концентрация образующихся при этом свободных радикалов, в то время как концентрация кумола в исходной смеси уменьшается. Относительным понижением скорости реакции 7 с повышением начальной концентрации гидроперекиси кумола в исходной смеси может быть убедительно объяснено весьма значительное понижение концентрации С14 в диметилфенил-карбиноле, образующемся при разложении этой гидроперекиси в меченом кумоле. [3]
Однако с увеличением начальной концентрации гидроперекиси скорость распада существенно возрастает. [4]
При изотермическом оформлении процесса начальная концентрация гидроперекиси также мала. Разбавителем служит какое-нибудь относительно легкокипящее вещество; на практике применяют один из продуктов реакции - ацетон. Реакция протекает при кипении реакционной смеси; изотермичность обеспечивается путем добавления к технической гидроперекиси ( перед поступлением в реактор) такого количества ацетона, чтобы смесь, образовавшаяся после разложения гидроперекиси, кипела при заданной температуре. Отвод тепла реакции осуществляется весьма эффективно и просто с помощью возвратного ацетона. [5]
Установлено, что с повышением начальной концентрации гидроперекиси кумола повышается, стремясь к некоторому пределу, значение кажущейся энергии активации ее термического разложения. [6]
Показано, что селективность окисления углеводорода не зависит от начальной концентрации введенной чужой гидроперекиси, а заниснт только от степени окисления самого углеводорода. [7]
Показано, что селективность окисления углеводорода не зависит от начальной концентрации введенной чужой гидроперекиси, а: зависит только от степени окисления самого углеводорода. [8]
Рисунки 88 и 89 демонстрируют влияние температуры, катализатора и начальной концентрации гидроперекиси на кинетику хемилюминесценции на начальной стадии реакции. Согласно рис. 88, повышение температуры приводит к увеличению начальной ( / нач) и максимальной ( / Макс) интенсив-ностей свечения. Скорость достижения максимальной интенсивности свечения при этом также возрастает. [9]
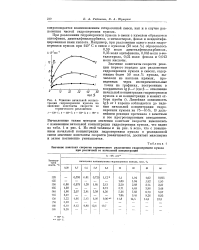 |
Влияние начальной концентрации гидроперекиси кумола на значение константы скорости ее термического разложения. [10] |
Из этой таблицы и из рис. 4 ясно, что с повышением начальной концентрации гидроперекиси кум: ола в реакционной смеси значение константы скорости увеличивается, достигает максимума и затем постепенно уменьшается. [11]
Авторы работы [12] установили, что разложение чистой гидроперекиси кумола протекает с самоускорением, а в смеси ее с кумолом ( начальная концентрация гидроперекиси кумола 25, 50 и 75 %) реакция, по их мнению, имеет нулевой порядок относительно гидроперекиси. В другой работе [13] было показано, что процесс разложения гидроперекиси кумола в кумоле даже при весьма значительной начальной концентрации удовлетворительно описывается кинетическим уравнением реакции первого порядка. Там же отмечается, что с повышением начальной концентрации гидроперекиси кумола увеличивается значение константы скорости ее разложения. [12]
Кинетика распада гидроперекисей в растворах имеет сложный характер, зависящий от условий протекания процесса. С изменением начальной концентрации гидроперекиси изменяется порядок реакции распада. [13]
С ростом начальной концентрации гидроперекиси кумола в ее смеси с кумолом сильно повышается скорость ее разложения, а следовательно, увеличивается концентрация образующихся при этом свободных радикалов, в то время как концентрация кумола в исходной смеси уменьшается. Относительным понижением скорости реакции 7 с повышением начальной концентрации гидроперекиси кумола в исходной смеси может быть убедительно объяснено весьма значительное понижение концентрации С14 в диметилфенил-карбиноле, образующемся при разложении этой гидроперекиси в меченом кумоле. [14]
Из температурной зависимости констант скорости реакции были вычислены значения кажущейся энергии активации Е разложения гидроперекиси кумола в различных растворителях, которые приведены в той же таблице. Результаты нашего исследования показывают, что с увеличением начальной концентрации гидроперекиси увеличивалась кажущаяся энергия активации ее разложения. [15]
Страницы: 1 2