Начальная концентрация - гидроперекись
Cтраница 2
Если начальная концентрация гидроперекиси была невысокой ( не выше 0 1 мол / л), то во всех растворителях ( за исключением к-нонана) реакция имела первый порядок. Эта закономерность сохранялась до 75 - 85 % падения начальной концентрации гидроперекиси, после чего наблюдалось заметное торможение реакции. [16]
Константа Михаэлиса Км ( &2 ka) / ki представляет собой константу диссоциации комплекса Мо - ГПЭБ. Найденная графически из зависимости 1 / W - 1 / [ ГПЭБ ] при начальных концентрациях гидроперекиси она оказалась равной 90 96 моль / л, тогда как константа скорости определяющей стадии ka 1 39 л / моль - сек. Графическое определение констант диссоциации комплексов Мо-вода иМо - метилфенилкарбинол показало, что ингибирование реакции водой в 25 - 26 раз сильнее, чем метилфенилкарбинолом. Наиболее активным ингибитором признана вода, эффект ингибирования которой в 12 - 25 раз больше, чем у спиртов, образующихся при распаде гидроперекисей. При исследовании относительной ингибирующей активности спиртов различного строения найдена корреляция полярных факторов по Тафту ( а) с константами диссоциации комплексов этих спиртов с катализатором. [17]
Показано, что в смесях, содержащих не более 50 мол. Вычисленное по этому закону значение константы скорости реакции сначала увеличивается, достигает максимума, а потом уменьшается с повышением начальной концентрации гидроперекиси ку-мола в смеси ее с кумолом. [18]
Авторы работы [12] установили, что разложение чистой гидроперекиси кумола протекает с самоускорением, а в смеси ее с кумолом ( начальная концентрация гидроперекиси кумола 25, 50 и 75 %) реакция, по их мнению, имеет нулевой порядок относительно гидроперекиси. В другой работе [13] было показано, что процесс разложения гидроперекиси кумола в кумоле даже при весьма значительной начальной концентрации удовлетворительно описывается кинетическим уравнением реакции первого порядка. Там же отмечается, что с повышением начальной концентрации гидроперекиси кумола увеличивается значение константы скорости ее разложения. [19]
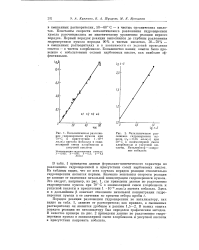 |
Каталитическое разложение гидроперекиси кумола при 70 С в присутствии 1 10 - 3 моль / л ацетата кобальта в эквимолярной смеси хлорбензола л уксусной кислоты. [20] |
В табл. 1 приведены данные формально-кинетического характера по разложению гидроперекисей в присутствии солей карбоновых кислот. Из таблицы видно, что во всех случаях порядок реакции относительно гидроперекиси является первым. Значение константы скорости реакции не зависит от изменения начальной концентрации гидроперекиси кумола. Это следует, например, из рис. 1, где приведены данные по разложению гидроперекиси кумола при 70 С в эквимолярной смеси хлорбензола и уксусной кислоты в присутствии 1 10 - 3 молъ / л ацетата кобальта. [21]
 |
Спектр ЭПР, фиксируемый при разложении / п йт-бутилгидроперзкиси в хлорбензоле в присутствии абиетата кобальта. [22] |
Пероксирадикалы генерируются и расходуются в процессе разложения гидроперекиси. Поэтому, исследуя, как меняется интенсивность сигналов ЭПР в ходе каталитического разложения гидроперекиси в зависимости от условий проведения реакции, можно делать определенные суждения относительно ее механизма. В работе 7 нами были приведены данные исследования влияния на интенсивность сигнала ЭПР начальной концентрации гидроперекиси, природы гидроперекиси, а также растворителя. [23]
Специальными исследованиями по методу 10 было показано, что в данном случае в восстановлении принимают участие два электрона. На опыте получаются несколько меньшие значения. В водном растворе опытное значение числа электронов, участвующих в восстановлении грег-бутилгидроперекиси, несколько зависит от начальной концентрации гидроперекиси. [24]
Специальными исследованиями по методу10 было показано, что в данном случае в восстановлении принимают участие два электрона. На опыте получаются несколько меньшие значения. В водном растворе опытное значение числа электронов, участвующих в восстановлении грег-бутилгидроперекиси, несколько зависит от начальной концентрации гидроперекиси. [25]
 |
Зависимость концентраций продуктов радиоли-за гидроперекиси изооктила от дозы ( мощность дозы 2 4 - 1016 эв / мл-сек, температура 0, исходная концентрация гидроперекиси. [26] |
При высоких концентрациях ROOH сразу происходит образование диалкилперекисей. При промежуточных концентрациях происходит дополнительное образование гидроперекисей и только при достижении определенной концентрации ROOH начинается образование диалкилперекисей. При этом наблюдается образование дополнительных количеств спиртов, а накопление карбонильных соединений не зависит от начальной концентрации гидроперекисей в растворе. Указанные закономерности наблюдались в системах гидроперекись вторичного гептила - гептан - кислород и гидроперекись 2 2 4-три-метилпентила - 2-изооктан-кислород. [27]
Если начальная концентрация гидроперекиси была невысокой ( не выше 0 1 мол / л), то во всех растворителях ( за исключением к-нонана) реакция имела первый порядок. Эта закономерность сохранялась до 75 - 85 % падения начальной концентрации гидроперекиси, после чего наблюдалось заметное торможение реакции. В анизоле, кумоле, фенилцик-логексане и в диизопропилбензоле реакция имела первый порядок независимо от величины начальной концентрации гидроперекиси. Так, в смеси г-идроперекиси кумола в кумоле первый порядок реакции по гидроперекиси удовлетворительно соблюдался даже при начальной ее концентрации порядка 30 - 45 мол. [28]
Это говорит о том, что изменение концентрации гидроперекиси при ее распаде описывается уравнением первого порядка. Действительно, при растворении полимера в нафталине или цетане скорость распада гидроперекиси по-прежнему остается пропорциональной первой степени ее концентрации, но константа скорости распада, вычисленная по уравнению первого порядка, изменяется пропорционально степени разбавления. Причем, как видно из табл. 2, константа определяется только степенью разбавления и не зависит от начальной концентрации гидроперекиси. [29]
По мере разложения гидроперекиси в реакционной смеси появляются фенол и ацетон. Величина основности ацетона больше, чем величины основности фенола и гидроперекиси, поэтому большая часть присутствующей кислоты связана с ацетоном. Комплекс, образованный ацетоном и кислотой, должен обладать меньшей каталитической активностью, чем свободная кислота, и в связи с этим должна уменьшиться скорость разложения гидроперекиси. Аналогично можно объяснить влияние добавок эквимолярных количеств фенола и ацетона на скорость реакции в том случае, когда концентрация добавки соизмерима с начальной концентрацией гидроперекиси. После начальной стадии реакции, характеризующейся повышенной скоростью, процесс протекает так, что его ход удовлетворительно описывается кинетическим уравнением реакции первого порядка. [30]
Страницы: 1 2