Электронная концентрация
Cтраница 3
Так как электронная концентрация по существу не зависит от температуры, то все изменение удельного сопротивления р с температурой должно быть обусловлено изменением подвижности. Если бы кристаллическая решетка металла не имела отклонений от идеальной периодичности, то носители тока не претерпевали бы рассеяния и подвижность электронов была бы бесконечно большой. В действительности периодичность решетки нарушается химическими примесями к физическими дефектами - в этом случае подвижность не зависит от температуры. Но нарушение периодичности может быть вызвано также небольшими перемещениями ионов в результате теплового движения; в этом случае подвижность уменьшается, при возрастании температуры. [31]
 |
Области существования фаз типа 6, ( х, Р и R в трехкомпонентных системах ( в ат. %. [32] |
Пунктиром показана электронная концентрация. [33]
Поэтому понятия электронной концентрации и концентрации электронов приводимости не всегда совпадают. У щелочных и щелочно-земельных металлов валентные электроны полностью отданы в коллективное пользование. Однако прочность связи в кристаллах rf - элементов значительно выше за счет усиления ковалентного взаимодействия, обусловленного возникновением d - rf - связей. Таким образом, эти элементы обладают в кристаллическом состоянии не чисто металлической, а ковалентно-металлической связью. [34]
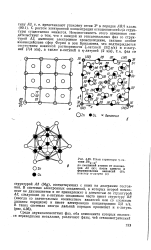 |
План структуры f - ла-туни D8t 3. [35] |
С ростом электронной концентрации отношение осей с / а структуры существенно меняется. [36]
При подсчете электронной концентрации надо иметь в виду, что в разных соединениях один и тот же элемент может иметь различную валентность. Так, например, элементы VIII-а подгруппы обычно имеют валентность, равную нулю, но в некоторых соединениях они одновалентны ( например, ВеСо, № 3Sn и др.) и даже двувалентны. [37]
Подобному увеличению электронной концентрации в валентной зоне до 40 % соответствует предельная растворимость металлов в серебре; например, твердый раствор на основе серебра может содержать ( мол. [38]
При подсчете электронной концентрации надо иметь в виду, что в разных соединениях один и тот же элемент может иметь различную валентность. Так, например, элементы VIII-a подгруппы в интерметаллических соединениях обычно имеют валентность, равную нулю, но в некоторых соединениях они одновалентны ( в ВеСо, NisSn и др.) и даже двухвалентны. [39]
 |
Области преобладания различных видов ушнрения по и. [40] |
При снижении электронной концентрации допплеровское уширение становится сравнимым со штарковским. Это наиболее характерно для высоких давлений, легких элементов и линий, возникающих при переходах с низко расположенных уровней. На рис. 1 для некоторых частных случаев показаны области, в которых преобладают различные виды уширения. [41]
Поэтому понятия электронной концентрации и концентрации электронов проводимости не всегда совпадают. У щелочных и щелочно-земельных металлов валентные электроны полностью отданы в коллективное пользование. Однако прочность связи в кристаллах rf - элементов значитель - но выше за счет усиления ковалентного взаимодействия, обусловленного возникновением d - rf - связей. Таким образом, эти элементы обладают в кристаллическом состоянии не чисто металлической, а ковалентно-металлической связью. [42]
Критическая величина электронной концентрации выводится кз условий заполнения электронами зон дозволенных энергий для данного кристалла. Если имеются две кристаллические структуры А и В и первая зона Бриллюэна ( см. гл. II) заполняется раньше для Л, то с этого момента более устойчивой делается структура В. После заполнения первой зоны для кристаллической решетки твердого раствора эта решетка становится неустойчивой и дальнейшее увеличение концентрации электронов должно привести к скачкообразному изменению: возникает другая решетка, для которой величина электронной концентрации, отвечающей заполнению зоны, выше. Роль электронной концентрации осложняется действием размерного фактора. Это условие не всегда соблюдается, особенно при большом различии в валентности. Однако на основе анализа электрического сопротивления макрообразца сплава Мотт показал, что избыточный заряд, остающийся на растворенном атоме, невелик. [43]
В понижает электронную концентрацию, и в валентной зоне появляются свободные энергетические состояния. [44]
Они имеют определенную электронную концентрацию ( отношение числа валентных электронов к числу атомов) и отличную от компонентов кристаллическую решетку. Соединения этого типа характерны для сплавов меди-латуни ( CuZn), оловянистых ( Cu3Sn), алюминиевых и бериллиевых бронз. [45]
Страницы: 1 2 3 4