Активная концентрация
Cтраница 3
Электродный потенциал при активной концентрации ионов металла в растворе, равной единице, называется нормальным потенциалом и обозначается EQ. Нормальные потенциалы большинства металлов и окислительно-восстановительных систем определены по отношению к водородному электроду, и их можно найти в соответствующих таблицах. [31]
С другой стороны, активная концентрация Мп определяется равновесиями образования гидроксоформ в растворе. [32]
По мере экстрагирования уменьшается активная концентрация экстрагента и изменяется коэффициент активности Yopr, в результате чего уменьшается коэффициент распределения. При экстрагировании больших количеств изменение коэффициента распределения может быть связано с ограниченной растворимостью экстрагируемого соединения в экстрагенте. При экстрагировании нескольких компонентов может быть их взаимное влияние на коэффициент распределения. На коэффициенте распределения сказывается присутствие в растворе веществ, связывающих реагент или экстрагент. [33]
В случае, если активная концентрация ионов металла в растворе равна единице, потенциал условно называется нормальным или стандартным. [34]
В зависимости от соотношения активных концентраций FeO и МпО в шлаке равновесие реакции может быть смещено в ту или другую сторону. [35]
По данным А.И. Даниленко [47], активная концентрация радиоактивного 40К в крови человека составляет 1.6 - КГ1 - 3 64 - 10 - 18 кюри / мл. [36]
Этот вывод совершенно неверен; активная концентрация ионов С1 - будет больше удвоенной активной концентрации ионов Ва4 1, так как свобода передвижения двух-зарядного иона бария сильнее ограничена, чем однозарядного иона хлора. Причем сами обозначения вэ44 ci - ошибочны, так как они не соответствуют ни концентрациям, ни активностям этих ионов. [37]
Таким образом может быть изменена активная концентрация замедлителя и ионный состав воды. [38]
 |
Влияние свойств и параметров ионообменной системы на равновесное распределение ионов. [39] |
Сдвигу равновесия вправо способствует уменьшение активной концентрации ( активности) иона А и увеличение активности иона В в растворе, чем бы это явление ни было вызвано. [40]
 |
Датчик индуктив - Достаточной прово-ного концентратомера, ра - ДИМОСТИ в емкостной встающего на частоте 50 гц. цепи.| Емкостный датчик. а - принципиальная. [41] |
Я - потенциал электрода при активной концентрации его ионов в растворе, равной единице; Л - универсальная газовая постоянная, равная8 31 дж; Т - абсолютная темп-ра; F - число Фарадея ( 96500 кулонов); ан - активная концентрация ионов водорода. Для измерения активной концентрации водородных ионов необходим электрод, закономерно изменяющий свой потенциал в зависимости от концентрации водородных ионов. Такими электродами являются: ме-таллооксидные ( сурьмяный, висмутовый, молибденовый, вольфрамовый) и стеклянный. Ни один из металлооксидных электродов не универсален в широком диапазоне значений рН и темп-р. Шире применяют стеклянный электрод ( рис. 1, а), позволяющий измерять концентрацию ионов водорода во многих растворах различного химич. Весь диапазон измерения величины рН ( от - 2 до 14) при температурах от 0 до 100 С охватывается посредством ряда электродов, отличающихся друг от друга маркой электродного стекла. [42]
Нормальный электродный потенциал возникает при активной концентрации ионов в растворе его соли, равной 1 г-ион на литр. [43]
Влияние величины рН, определяющей активную концентрацию в воде гидроксиль-ных ионов, следует из механизма процесса обескремнивания. [44]
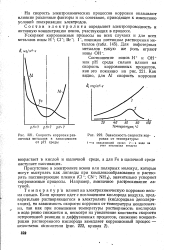 |
Скорость коррозии различных металлов в зависимости от рН среды.| Зависимость скорости коррозии от температуры. [45] |
Страницы: 1 2 3 4