Активная концентрация
Cтраница 4
Состав электролита определяет электропроводность и активную концентрацию ионов, участвующих в процессе. [46]
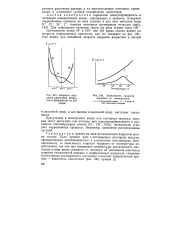 |
Скорость коррозии различных металлов в зависимости от рН среды.| Зависимость скорости коррозии от температуры. [47] |
Состав электролита определяет электропроводность и активную концентрацию ионов, участвующих в процессе. [48]
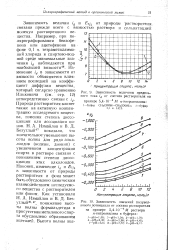 |
Зависимость величины предельного тока id от состава растворителя на. [49] |
Природа растворителя влияет также на активную концентрацию исследуемого вещества, изменяя степень диссоциации или ассоциации ионов. Наконец, изменение id и Ei / 2 в зависимости от природы растворителя и фона может быть обусловлено химическим взаимодействием исследуемого вещества с растворителем или фоном. Как установили Н. А. Измайлов и Безуглый49 - 47, понижение высоты волны формальдегида в присутствии метилового спирта обусловлено образованием ацеталей. [50]
При значительной концентрации сильного электролита его активная концентрация существенно отличается от истинной. Поэтому в таких случаях нужно вводить поправку на активность электролита. [51]
Под влиянием ионов Na и СК активная концентрация - активность ионов Са и С2О4 как бы понижается. Для того чтобы вычислить эту активную концентрацию, надо умножить обычную ( аналитическую) концентрацию на так называемый коэффициент активности - дробь, показывающую, какая часть из общего числа ионов свободна. Таким образом, в более точном выражении произведение растворимости равно не произведению концентраций, а произведению активностей. [52]
Иногда вместо слова активность используют выражение активная концентрация, хотя такой термин нельзя считать вполне корректным. [53]
Строго говоря, Ко равен отношению активных концентраций вещества в обеих фазах. Но поскольку хроматографиро-вание проводят в разбавленных растворах, которые можно считать идеальными, то можно использовать отношение концентраций. Коэффициент распределения зависит от природы вещества, природы растворителя и температуры. [54]
Таким образом, получена зависимость произведения активных концентраций ионов Са2 и SO. [55]
Произведение растворимости в действительности равно произведению активных концентраций ионов. Поэтому сравнивать с ним нужно не произведение действительных концентраций ионов, а величину, предварительно умноженную на коэффициенты активностей соответствующих ионов. [56]
Моль СаС12 111 г. Для определения активной концентрации электролита необходимо знать его моляльную концентрацию. [57]
В том случае, когда произведение активных концентраций ионов Са2 и SO J - будет превышать 2 4 - Ю-5, необходимо предусматривать продувку системы оборотного водоснабжения. Величина продувки, а следовательно, и коэффициент упаривания должны быть такими, при которых произведение активных концентраций Са2 и S0 - будет равно 2 4 - Ю-5. Величина коэффициента упаривания, при которой соблюдается это условие, определяется методом подбора. По определенному подбором коэффициенту упаривания исходя из заданного уноса капельной влаги, испарения и утечек определяется размер продувки. [58]
Страницы: 1 2 3 4