Общая концентрация - вещество
Cтраница 1
Общая концентрация вещества С позволяет вычислить теоретически возможное количество ионов, которое может образоваться при полном распаде всех молекул растворенного вещества на ионы. [1]
Обозначим общие концентрации веществ АХ и ВХ через а и Ь, а концентрации их изотопных разновидностей АХ и ВХ через х и у. [2]
Коэффициент распределения вьфажает отношение общей концентрации вещества в одной жидкой фазе к его концентрации во второй фазе в условиях равновесия. [3]
Значение KN зависит от общей концентрации веществ в неидеальном растворе. [4]
Коэффициент распределения D равен отношению общей концентрации вещества в органической фазе к его концентрации в водной фазе. [5]
С другой стороны, с изменением общей концентрации вещества может изменяться число поглощающих частиц данного вида в результате полимеризации или диссоциации. [6]
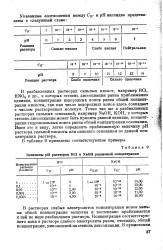 |
Величины рН растворов НС1 и NaOH различной концентрации. [7] |
В растворах слабых электролитов концентрация ионов меньше общей концентрации вещества и постепенно приближается к ней по мере разбавления раствора. Концентрация соответствующего иона в растворе слабого электролита равна, очевидно, общей концентрации, умноженной на степень диссоциации. [8]
После того как был пропущен объем раствора At, пусть общая концентрация вещества в упомянутой тарелке будет р дв. [9]
Последнее уравнение показывает, что величина полимеризованной фракции зависит от общей концентрации вещества А. [10]
Последнее уравнение показывает, что величина полимеризо ванной фракции зависит от общей концентрации вещества А. [11]
Как правило, при использовании кинетических методов анализа определяют равновесную, а не общую концентрацию вещества, поэтому указанные методы с успехом можно применять при изучении равновесий в растворах и, в особенности, при изучении равновесий реакций образования комплексных соединений. [12]
 |
Схема разделения компо-не гов Л я В при элюи-ровании. [13] |
Обычно разделяемые ионы появляются в вы-текающем потоке с концентрациями, составляю-щими чаще всего небольшую часть от общей концентрации элюирующего вещества Со - Продукт, используемый обычно в качестве элюирующего агента, не мешает дальнейшей обработке разделенных фракций. [14]
Когда мы по экспериментальным данным определяем коэффициенты активности ионов, то мы всегда фактически наблюдаемые свойства ионов относим к общей концентрации вещества, а не к его ионизированной части. [15]
Страницы: 1 2 3 4