Общая концентрация - вещество
Cтраница 3
Константа К постоянна только в том случае ( при постоянной температуре), если соединение в обеих фазах рассматриваемой области концентраций находится в одной и той же молекулярной форме. Если протекают процессы диссоциации или ассоциации молекул и если вводят в уравнение ( вследствие незнания этих равновесий) вместо с0 или си аналитически определяемую общую концентрацию, то отношение CQ / CU уже He-будет постоянным. Концентрацию молекул определенного вида можно в этом случае выразить как функцию общей концентрации вещества в соответствующей фазе, если известны все равновесия и их константы. [31]
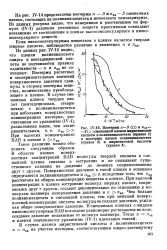 |
Изотермы п - S ( О и яад - - S ( х смешанной пленки миристиновой кислоты и поливинилацетата ( кривая 1 и изотермы пленок поливинилацетата ( кривая 2 и миристиновой кислоты ( кривая 3. [32] |
В области низких поверхностных концентраций ПАВ молекулы твердой кислоты в смешанной пленке связаны в островки и не оказывают существенного влияния на давление до момента соприкосновения друг с другом. Поверхностное давление в такой пленке в основном определяется поливинилацетатом и яад я вследствие того, что яад рассчитана на общую концентрацию вещества в пленке. Чем больше поливинилацетата в смешанной пленке, тем при меньшей поверхностной концентрации кислоты молекулы ее создают давление, усиливая общее поверхностное давление. В смешанных пленках с жидким низкомолекулярным ПАВ последние равномерно растекаются по воде, создавая давление независимо от молекул полимера. Тогда я пад и пленки подчиняются уравнению ( IV-1) идеальных смесей. [33]
При экстракции обычно имеются две несмешивающиеся фазы и одно распределяемое вещество. Следовательно, при постоянных температуре и давлении система монова-риантна. В условиях равновесия отношение концентраций распределяющегося вещества в обеих фазах ( с0 и св) - величина постоянная, не зависящая от общей концентрации вещества. [34]
Однако эти вещества отличаются величинами констант ионизации. Характеристическая растворимость 5, лауриновой кислоты очень мала; поэтому, хотя при рН рКа на 2 единицы ионизировано 99 % растворенной части вещества, раствор, общая концентрация вещества в котором составляет 0 001 М, яв ляется насыщенным. [35]
Чтобы разрешить это противоречие, Беляев предполагает, что мономолекулярная реакция в тех условиях ее течения, которые имеют место во фронте горения, превращается в бимолекулярную в том смысле, в каком это происходит со всеми мономолекулярными реакциями при очень низких давлениях. Как известно, кажущаяся независимость образования активированных молекул при мономолекулярных реакциях от числа соударений обусловливается тем, что при столкновении наряду с активацией идет также дезактивация активных молекул. Если время жизни активной молекулы велико по сравнению с временем между соударениями, то устанавливается некоторая определенная концентрация активных молекул, которой ( а через лее и общей концентрации вещества) пропорциональна скорость реакции. Это же дает пропорциональность скорости горения давлению. [36]
Общая скорость адсорбции складывается из скорости собственно адсорбции и скорости десорбции. При равновесии, когда в макроскопическом масштабе не протекает никакого процесса, скорость адсорбции равна скорости десорбции. В этом случае число частиц, адсорбирующихся на поверхности в единицу времени, равно числу частиц, покидающих поверхность за то же время. Таким образом, общая концентрация вещества ни на поверхности, пи в растворе не изменяется. [37]
Рассматриваемый закон распределения ( 1) и основное уравнение разделения двух компонентов ( 3) справедливы в условиях отсутствия протекания побочные, процессов. Среди этих последних основным является изменение активной концентрации экстрагирующейся формы каждого из разделяемых компонентов, часто не совпадающей с общей концентрацией каждого из них. В случае экстракции электролитов, заметно распадающихся на ионы в водных растворахиэкстрагирующихся в виде недиссоциированных молекул, концентрация экстрагирующейся формы ( не-продиссоциированной части вещества) будет меньше его общей концентрации. В случае электролитов закон распределения также соблюдается, если вместо общей концентрации вещества при расчете коэффициента распределения пользоваться концентрациями экстрагируемой формы. В случае почти полной диссоциации вещества, распадающегося с образованием двух ионов, концентрация этого вещества в экстракте линейно зависит от квадрата его общей концентрации в воде. [38]
Рассматриваемый закон распределения ( 1) и основное уравнение разделения двух компонентов ( 3) справедливы в условиях отсутствия протекания побочны, процессов. Среди этих последних основным является изменение активной концентрации экстрагирующейся формы каждого из разделяемых компонентов, часто не совпадающей с общей концентрацией каждого из них. В случае экстракции электролитов, заметно распадающихся на ионы в водных растворах и экстра тирующихся в виде недиссоциированных молекул, концентрация экстрагирующейся формы ( не-продиссоциированной части вещества) будет меньше его общей концентрации. В случае электролитов закон распределения также соблюдается, если вместо общей концентрации вещества при расчете коэффициента распределения пользоваться концентрациями экстрагируемой формы. В случае почти полной диссоциации вещества, распадающегося с образованием двух ионов, концентрация этого вещества в экстракте линейно зависит от квадрата его общей концентрации в воде. [39]
Одним из факторов, ограничивающих возможность разделения концентрированных растворов обратным осмосом, является концентрационная поляризация, заключающаяся в накоплении задерживаемых веществ у поверхности мембраны со стороны высокого давления. Частично эти вещества вследствие селективности мембран проникают с фильтратом, но в основном диффундируют навстречу поступающему раствору. Поляризация снижает осмотическое давление, что при постоянном рабочем давлении снижает выход фильтрата. Повышение концентрации веществ около мембраны может привести к пересыщению раствора и выпадению осадка на мембране с вытекающими из этого последствиями Снижению концентрационной поляризации способствуют понижение общей концентрации удаляемых веществ в воде ( продувки камеры) и турбулизация потока в камере. Однако максимальная производительность мембраны и в этих условиях ограниченна. [40]
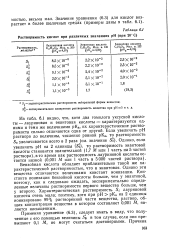 |
Растворимость кислот при различных значениях рН ( при 20 С. [41] |
Бензойная кислота обладает приблизительно такой же характеристической растворимостью, что и энантовая. Однако эти вещества отличаются величинами констант ионизации. Характеристическая растворимость S - лауриновой кислоты очень мала; поэтому, хотя при рН рКа на 2 единицы ионизировано 99 % растворенной части вещества, раствор, общая концентрация вещества в котором составляет 0 001 М, является насыщенным. [42]
При постоянных температуре и давлении равновесные концентрации не изменяются во времени сколь угодно долго. Равновесная концентрация вещества зависит от его общей или исходной концентрации и расхода вещества на протекание химической реакции или реакций до установления равновесия. Общая концентрация вещества в растворе обычно обозначается как с, а равновесная - как с, нередко в качестве символа равновесной концентрации используют также квадратные скобки [ ], в которые заключают формулу вещества. В растворе устанавливается равновесие между всеми формами существования вещества В. Сумма всех равновесных форм будет равна общей концентрации вещества В в растворе. [43]
Согласно классической теории электролитической диссоциации, созданной в 80 - х годах прошлого столетия Сванте Аррениусом, некоторая часть электролита, растворенного в воде, распадается на электрически заряженные частицы - ионы. Эти частицы в растворе проявляют индивидуальные свойства и в отличие от молекул, из которых они получились, могут принимать участие в реакциях. Поэтому скорость химической реакции, протекающей в растворе, определяется концентрацией не всего растворенного вещества, а только концентрацией образовавшихся из него ионов, которые и составляют как бы активную часть всего вещества. Отсюда вытекает важность представления о степени диссоциации. Степенью электролитической диссоциации а называется отношение концентрации вещества, распавшегося на ионы, к общей его концентрации в растворе. Общую концентрацию вещества в растворе часто называют аналитической концентрацией. [44]
Разумеется, второй конец колонки при этом открыт так, что жидкость между гранулами по всей ее длине приходит в движение. Как поведет себя зона. На переднем по течению жидкости крае зоны подвижная фаза, покидая область равновесия, начнет поступать в прилежащий участок колонки, где неподвижная фаза еще свободна от вещества. Молекулы последнего начнут диффундировать внутрь гранул неподвижной фазы, и будет устанавливаться новое равновесие между подвижной и неподвижной фазами на этом участке. Зона начнет расширяться, однако концентрация вещества в присоединяющемся спереди участке будет ниже, чем в исходной зоне, так как в этот участок поступает только то количество вещества, которое раньше содержалось в подвижной фазе такого же ( по длине колонки) участка. В это же время из точно такого же по длине колонки участка, находящегося в конце зоны, подвижная фаза уходит вперед, а на ее место поступает чистый элюент. И здесь происходит равновесное перераспределение, на этот раз за счет вещества, прежде находившегося в неподвижной фазе, которое теперь частично десорбируется. Общая концентрация вещества в этом арьергардном участке зоны, очевидно, тоже начинает уменьшаться. В остальных участках, на которые можно мысленно разбить исходную зону, уходящая вперед подвижная фаза замещается точно таким же раствором подвижной фазы, поступающим из расположенных сзади участков, и равновесие не нарушается. [45]
Страницы: 1 2 3 4