Наблюдаемая концентрация
Cтраница 2
Принципиально распределение может быть записано через любые примесные центры, какой бы малой ни была их относительная концентрация, но при условии, что учитываются все внутренние равновесия и наблюдаемая концентрация приравнивается сумме рассчитанных концентраций различных центров. Для того чтобы рассматривать распределение исходя только из одного центра ( пренебрегая всеми остальными), нужно быть уверенным, что выбранный центр представляет большинство атомов данной примеси. [16]
 |
Кинетические уравнения реакций для модели анаэробного фильтра. [17] |
Вследствие того что в модели анаэробного фильтра сопротивление переносу массы через биопленку не учитывалось, при оценке системы анаэробного фильтра может быть использовано более простое кинетическое уравнение первого порядка, учитывающее изменение наблюдаемой концентрации биомассы. [18]
В реальных условиях, когда вследствие конкурирующего комплексообразования реакция образования окрашенного комплекса с определяемым элементом протекает не до конца, ее чув-ствительнрсть определяется такой общей ( начальной) концентрацией анализируемого иона, при которой возможно образование окрашенного комплекса минимальной наблюдаемой концентрации. [19]
Тот факт, что Вселенная в прошлом проходила через состояние с темп-рой Т - 103 К, следует из существования в настоящее время изотропного микроволнового фонового излучения ( реликтового излучения) со строго тепловым ( планковским) спектром, а наличие темп-р Т - 10 - 1010 К ( 100 кэВ - 1 МэВ) в еще более ранний момент - из теории космологич, нуклеосинтеза, дающей правильные значения для наблюдаемых концентраций дейтерия, гелия-3, гелия-4 и лития-7. Дальнейшая экстраполяция в прошлое, в область более высоких энергий, плотностей энергии и темп-р, следует из ур-ний классич. Согласно этой теории, С. [20]
Проведенное сопоставление с экспериментальными данными показывает, что удается удовлетворительно объяснить наблюдаемые концентрации свободных радикалов ( в частности атомов азота) при гелиевых температурах с помощью теплоце-почечной модели. Реально же наблюдаемые концентрации радикалов при более высоких температурах ( в частности в органических соединениях) на 1 - 2 порядка ниже предсказываемых полученными формулами. [21]
Они имеют тот же порядок, что и наблюдаемые концентрации, и показывают, какое значение вымывание осадками имеет для химии дождя. Для сравнения с наблюдаемыми концентрациями отдельных примесей следует считать, что в континентальных аэрозолях растворимой является только часть аэрозольного вещества и что гигантские частицы под облаком удаляются достаточно быстро. [22]
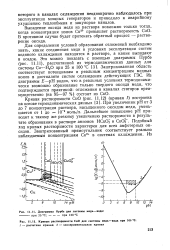 |
Диаграмма Пурбе для системы медь-вода.| Кривые растворимости СиО для системы медь-вода при 100 С. / - расчетная кривая. 2 - экспериментальная кривая. [23] |
Подобный ход кривых растворимости характерен для всех амфотерных оксидов. Заштрихованный прямоугольник соответствует реально наблюдаемым концентрациям Си2 в системах охлаждения. [24]
При исследованиях элементарных актов, позволяющих установить сечения ( или вероятности) тех или иных процессов, решается динамическая задача При рассмотрении эволюции функций распределения во времени ( а в случае неоднородной системы и в пространстве) необходимо воспользоваться уравнением Больцмана или какой-либо его линеаризованной или упрощенной формой. Наконец, при описании процесса в терминах наблюдаемых концентраций и скоростей необходимо применять управляющее уравнение, или уравнение Паули, являющееся обобщением основного уравнения обычной химической кинетики. Уравнение Паули учитывает не только каналы различных химических реакций, но и переходы между квантовыми уровнями в реагирующих молекулах и особенности реакций с различных энергетических уровней. В силу эюго в уравнение Паули входят не суммарные коэффициенты ( константы) скоростей химических реакций, которые применяются в обычной химической кинетике, а коэффициенты скоростей с различных квантовых уровней. Все эти коэффициенты скоростей химических реакций, учитывая заселенности и ее кинетику, в совокупности позволяют определить коэффициент ( константу) скорости, определяемую по промежуточным и конечным продуктам реакции в обычном химическом кинетическом эксперименте. [25]
Однако, чтобы сделать какие-либо обобщения, необходимы дальнейшие исследования. Горхэм [28] отмечал, что для речных вод Австралии соответствие между наблюдаемыми концентрациями хлорида и вычисленными из анализов дождевой воды и речных стоков является достаточно хорошим, если предполагать, что сухое выпадение и захват частиц соли растительностью незначительны. До сих пор анализы почвы на Srso хорошо согласуются с отложением под действием дождя, однако пробы почвы берутся на открытой местности, и сравнение с данными по хлору не может быть решающим. Другим важным фактором является распределение частиц по размерам. Было бы очень желательно дальше исследовать этот вопрос. [26]
 |
Гидрогенизация на платине. а - изопропилацетилена, б - фе-нилацетилена ( Лебедев. / - исходное вещество. 2 - промежуточное соединение. 3 - продукт реакции. [27] |
Уравнения (5.16) и (5.17) - это в точности уравнения Лебедева и Штерна [121], при интегрировании которых получаются уравнения, применение которых к гидрированию изопропилацетилена ( а 0 27) и фе-нилацетилена ( а 0 14) над платиной дает полное совпадение с опытом. Это видно из рис. 9, взятого из цитированных выше работ [121, 134]; на нем точки - наблюдаемые концентрации ацетиленового, этиленового и предельного соединений, а линии - вычисленные концентрации. [28]
Член г объединяет все константы скорости и константы равновесия, а ас - это произведение или более сложная зависимость всех концентраций в уравнениях ( 8) и ( 9), за исключением [ С ] 0 и [ R ] в числителе. Можно поддерживать величину ас постоянной в процессе измерения скорости, поскольку вещества, концентрация которых входит в ас, включая субстрат S, можно взять в большом избытке. Член [ R ] 0 выражает начальную концентрацию вещества, которое изменяет свою концентрацию в процессе реакции, a ( IR ] 0 - х) - наблюдаемая концентрация [ R ] в любой момент времени t после начала реакции. [29]
А между тем относительная чувствительность фотометрического определения, достигаемая в присутствии мешающих ионов, может существенно уменьшаться по сравнению с раствором чистой соли. В реальных условиях, когда вследствие конкурирующего ком-плексообразования реакция образования окрашенного комплекса с определяемым элементом протекает не до конца, ее чувствительность определяется такой общей ( начальной) концентрацией анализируемого иона, при которой возможно образование окрашенного комплекса минимальной наблюдаемой концентрации. [30]
Страницы: 1 2 3