Высокая концентрация - ион - водород
Cтраница 1
Высокая концентрация ионов водорода и ионов галоида приводит к тому, ЧТОБ этих условиях происходит быстрая аномеризация как исходных соединений, так и образующихся гликозилгалогенидов. Поэтому при таком методе синтеза конфигурация гликозидного центра в исходных соединениях не существенна, а образующиеся гликозилгалогениды всегда представляют собой наиболее стабильные аномеры. Была разработана удобная в препаративном отношении модификация этого метода, позволяющая осуществлять синтез ацето-галогеноз в одну стадию; три этом исходят из свободного моно - или дисахарида42: сахар ацетилируют уксусным ангидридом в присутствии хлорной кислоты, после чего к реакционной смеси прибавляют рассчитанные количества фосфора, брома и воды. Образующийся бромистый водород реагирует с полным ацетатом сахара и с высоким выходом дает ацетогалогенозу. [1]
Раствор H2SiF6 обладает высокой концентрацией ионов водорода, по своей силе эта кислота не уступает серной. Как H2SiB 6, так и ее соли ядовиты. [2]
Раствор H2SiF6 обладает высокой концентрацией ионов водорода, по своей силе эта кислота не уступает серной. Как II2SiF6, так и ее соли ядовиты. [3]
В кислых растворах с высокой концентрацией ионов водорода [ Н ] равновесие сдвинуто влево, и индикатор переходит в кислотную форму. [4]
В среде кислорода в растворах с высокой концентрацией ионов водорода ( рН1 2) коррозия стали ШХ15 протекает со смешанной водородно-кислородной деполяризацией, причем потери железа от коррозии с водородной деполяризацией составляют около 57 % от общих коррозионных потерь. [5]
При спектрофотометрических исследованиях часто требуются растворы с высокой концентрацией иона водорода. Растворы эти легко получаются путем соответствующего разбавления соляной кислоты водой до необходимой концентрации, так как при этом может быть сделано допущение о полной ионизации соляной кислоты. [6]
Для количественного протекания реакции необходимо применение высокой температуры, высокой концентрации ионов водорода и высокой концентрации иодид-ионов. [7]
При растворении осадка в соляной кислоте нужно иметь в виду, что высокая концентрация ионов водорода может помешать в дальнейшем открытию и отделению Ва в виде хромата бария. Во избежание этого к солянокислому раствору добавляют ацетат натрия. [8]
Результаты расчетов показали, что в воздушной среде, в растворах с высокой концентрацией ионов водорода ( рй1 2) коррозия pg0f2 двтшмп ъеш поглощенно, стали ШП5 протекает прей - го кислорода от рН среда и ооотава мужественно с водородной газовой фазы: деполяризацией, потери ке - et - щг Р Д - аргон леза от нее составляют около 85 % от общих коррозионных потерь. При остальных исследованных значениях рН коррозия стали происходит преимущественно о кислородной диполяризацией, потери келеза от дав составляют 85 % ( при рН - 2 6) - 96 % ( при рН12 55) от суммарных коррозионных потерь. С ростом рН доля коррозии с кислородной деполяризацией увеличивается. J рассмотрены причины увеличения скорости коррозии келеза с кислородной деполяризацией и уменьшения скорости коррозии с водородной деполяризацией при трении о повышением рН растворов. [9]
 |
Кривые ток - потенциал для одноэлектронного восстановления церия ( 1У ( кривая А и железа ( ill. ( кривая Б на платиновом катоде в 1 F растворе серной кислоты. [10] |
При - 0 В на каждой кривой ток возрастает без кажущегося предела вследствие высокой концентрации ионов водорода. [11]
Следовательно, кажется целесообразным использовать ионную среду высокой концентрации, особенно, если требуется высокая концентрация ионов водорода или лиганда. В работах по гидролизу ионов металлов, например, часто нужно было использовать высокие концентрации ионов водорода для того, чтобы получить растворы, содержащие негидролизованные формы. [12]
Этерификация ускоряется в присутствии сильных минеральных кислот, так как в растворах таких кислот создается высокая концентрация ионов водорода, являющихся катализаторами реакции. По этой же причине этерификация спиртов сильными минеральными кислотами идет быстро. [13]
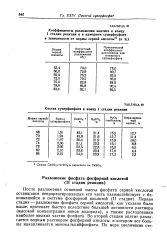 |
Состав суперфосфата к концу I стадии реакции. [14] |
Первая стадия - разложение фосфата серной кислотой, как указано было выше, протекает быстро вследствие большой активности раствора ( высокой концентрации ионов водорода), а также расходования наиболее мелких частиц фосфата. Во второй стадии апатит разлагается водным раствором фосфорной кислоты, в котором все больше накапливается монокальцийфосфата. [15]
Страницы: 1 2