Высокая концентрация - ион - водород
Cтраница 2
Аналогичные результаты были получены и при изучении гидролиза р-пропиолак-тона [ f02 ]; следует добавить, что в этом случае реакция, катализируемая кислотами, становится преобладающей только тогда, когда будет достигнута высокая концентрация ионов водорода. [16]
В щелочных растворах, характеризующихся очень небольшим значением [ Н ], это равновесие сдвинуто вправо и индикатор почти полностью превращается в щелочную форму ( синюю в случае лакмуса); в кислых растворах с высокой концентрацией ионов водорода [ Н / ] равновесие сдвинуто влево и индикатор переходит в кислую форму. [17]
Хорошими восстановителями являются жидкие амальгамы различных неблагородных металлов, таких, как цинк, кадмий, олово, свинец и висмут. Эти амальгамы при самой высокой концентрации ионов водорода не выделяют Н2, так как его выделение на ртути требует высокого перенапряжения. Позволяет раздельно определять многие окислители в растворе. [18]
Активным катализатором для обеих приведенных реакций-прямой и обратной-являются ионы водорода. Добавляемая серная кислота не только обеспечивает высокую концентрацию ионов водорода в смеси, но при достаточном ее количестве может одновременно связывать образующуюся при этерификации воду и сдвигать равновесие в сторону образования сложного эфира. [19]
Активным катализатором для обеих реакций - прямой и обратной - являются ионы водорода. Добавляемая серная кислота не только обеспечивает высокую концентрацию ионов водорода в смеси, но при достаточном ее количестве может одновременно связывать образующуюся при этерификации воду и сдвигать равновесие в сторону образования сложного эфира. [20]
Следовательно, кажется целесообразным использовать ионную среду высокой концентрации, особенно, если требуется высокая концентрация ионов водорода или лиганда. В работах по гидролизу ионов металлов, например, часто нужно было использовать высокие концентрации ионов водорода для того, чтобы получить растворы, содержащие негидролизованные формы. [21]
Этерификация спиртов органическими, а также слабыми минеральными кислотами идет очень медленно. Эта реакция ускоряется в присутствии сильных минеральных кислот, так как в растворах таких кислот создается высокая концентрация ионов водорода, являющихся катализаторами реакции этерификации. По этой же причине этерификация спиртов сильными минеральными кислотами идет быстро. [22]
 |
Скорость коррозии меди в неокисляющих кислотах. [23] |
В горячей концентрированной соляной кислоте, однако, медь довольно легко растворяется и с выделением водорода. В этом случае образуются комплексные ионы меди ( СиС12) - и потенциал ее сильно разблагораживается, а благодаря высокой концентрации ионов водорода делается: возможным протекание процесса водородной деполяризации. Рассмотренные электрохимические характеристики и определяют характер стойкости меди и медных сплавов. Однако наличие окислителей, таких, как HNO3), Н2О2, или даже продувание кислорода или воздуха через, эти растворы, заметно повышает скорость коррозии меда и медных сплавов. [24]
При действии на спирты кислот происходит выделение воды и образуются сложные эфиры. Этери-фикация спиртов органическими, а также слабыми минеральными кислотами идет очень медленно, так как в растворах таких кислот создается высокая концентрация ионов водорода, являющихся катализаторами реакции этерификации. [25]
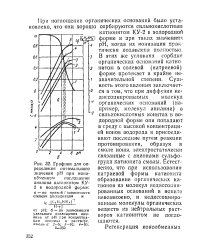 |
Графики для определения оптимального значения рН при ионообменном поглощении анилина катионитом КУ-2 в водородной форме. [26] |
У-2 в водородной форме и при таких значениях рН, когда их ионизация практически подавлена полностью. В этих же условиях сорбция органических оснований катио нитом в солевой ( натриевой) форме протекает в крайне незначительной степени. Сущность этого явления заключается в том, что при диффузии недиссоциированных молекул органических оснований ( например, молекул анилина) в сильнокислотных ионитах в водородной форме они попадают в среду с высокой концентрацией ионов водорода и присоединяют последние путем реакции протонирования, образуя в смоле ионы, электростатически связанные с анионами сульфо-групп катионита смолы. Естественно, что при использовании натриевой формы катионита образование органических катионов из молекул недиссоциированных оснований в ионите невозможно, и недиссоциированные молекулы органических веществ из нейтральных растворов катионитом не поглощаются. [27]
Однако при замыкании электродов картина меняется: коррозия электрода, помещенного в нейтральный электролит, резко возрастает. Последнее обусловлено тем, что электрод, омываемый нейтральным электролитом, становится анодом и на нем преимущественно протекают анодные процессы. Катодные же процессы в этом случае сосредоточиваются на электроде, находящемся в кислом пространстве. Потенциал этого электрода вследствие высокой концентрации ионов водорода и незначительной поляризации поддерживается на более положительном уровне. Скорость коррозии железного электрода, находящегося в нейтральном электролите, вследствие анодной поляризации увеличивается почти в б раз. [28]
Однако при замыкании электродов картина меняется: коррозия электрода, помещенного в нейтральный электролит, резко возрастает. Последнее обусловлено тем, что-электрод, омываемый нейтральным электролитом, становится анодом и на нем преимущественно протекают анодные процессы. Катодные же процессы в этом случае сосредоточиваются на электроде, находящемся в кислом пространстве. Потенциал этого электрода вследствие высокой концентрации ионов водорода и незначительной поляризации поддерживается на более положительном уровне. Скорость коррозии железного-электрода, находящегося в нейтральном электролите, вследствие анодной поляризации увеличивается почти в 6 раз. [29]
В присутствии некоторых веществ наблюдается разобщение окислительного фосфорилирования, при котором органический субстрат окисляется, но АТР не синтезируется, а гидролизуется до ADP и ионов фосфата. Разобщители окислительного фосфорилирования принадлежат к двум группам ионофоров: одни из них переносят протоны, а другие - ионы щелочных металлов. Поскольку отрицательный заряд таких анионов распределен по всей молекуле, они могут пересекать липидную часть митохондриальной мембраны в направлении увеличения электрического потенциала. При попадании в межмембранный объем с высокой концентрацией ионов водорода анионы трансформируются в недиссоциированную форму кислоты и в этой форме переносятся обратно в матрикс. Там от молекулы отщепляется протон, захваченный в межмембранном объеме. [30]
Страницы: 1 2