Высокая концентрация - щелочь
Cтраница 3
Хром в кислом растворе при низкой плотности тока растворяется в двухвалентном состоянии, образуя голубой раствор, но если плотность тока возрастает выше определенного значения, то анодный потенциал подымается, и хром начинает растворяться как шестивалентный, давая желтую хромовую кислоту, В щелочном растворе при низких плотностях тока кобальт и марганец ( а также железо при повышенных температурах высокой концентрации щелочи) растворяются анодно, как двухвалентные, но при возрастающих плоскостях тока появляются более высокие окислы ( FesO4, CosOt или МпОг) или даже также растворимые соединения, как фер-раты или манганаты. Гладкое анодное растворение металла в щелочном растворе требует, чтобы его окислы имели кислый характер. [31]
Известно, что при прямой щелочной конденсации гшшшр-гидрина с дифенилояпропаном протекают последовательные реакции этерификации дифекилолпропана и дегвдрохлорирогання его хяор-гвдриновых эфиров. Высокие концентрации щелочи на ранних стадиях процесса вызывают гидролиз эпихлоргидрина. [32]
Практически эти условия имеют место в заклепочных швах и вальцовочных соединениях, так как образование соединений этого рода сопровождается усилиями, превышающими предел текучести, а при эксплуатации в элементах этих соединений возникают еще и термические напряжения местного характера. Высокая концентрация щелочи в этих местах образуется при наличии неплотности, так как пропуск воды в месте неплотности будет сопровождаться выпариванием и повышением содержания щелочи. [33]
В отличие от методов повышения нефтеотдачи с применением щелочных растворов в данной технологии используют малообъемные оторочки концентрированных растворов щелочей в смеси с полимером в процессе закачивания сточной минерализованной воды. Благодаря высокой концентрации щелочи в закачиваемом растворе при взаимодействии с катионами кальция и магния пластовой воды идет внутрипластовое образование практически нерастворимых в воде осадков гидроокисей и карбонатов, которые частично закупоривают водопроводящие канала пласта. [34]
Образующийся непредельный кротоновый альдегид ( 2-бу-теналь) имеет характерный резкий запах. При высокой концентрации щелочи процесс уплотнения идет дальше и образуются высокомолекулярные окрашенные смолистые продукты. [35]
Образующийся непредельный кротоновый альдегид ( бу-тен-2 - аль) имеет характерный резкий запах. При высокой концентрации щелочи процесс уплотнения идет дальше и образуются высокомолекулярные окрашенные смолистые продукты. [36]
Это приводит к снижению степени ионизации определяемого элемента и таким образом увеличивает долю атомов определяемого элемента, способных к переходу, что дает рост интенсивности резонансных линий. При высоких концентрациях щелочи наблюдается некоторое уменьшение эмиссии за счет самопоглощения. Этот эффект особенно заметен для лития и натрия [9] и может быть сведен до минимума в работе при повышенном разбавлении. Калибровочные графики для щелочных металлов представляют собой прямую линию только в области низких концентраций, однако возможные отклонения от линейности не мешают использованию этого графика. [37]
По окончании кипячения мыльная масса отстаивается около двух часов. За счет высокой концентрации щелочи происходит разделение мыльного клея на ядро и подмыльный щелок. Щелок после отстаивания сливают в коробку и используют для омыления новых партий соапстоков. Оставшееся в котле после полной высол-ки соапсточное ядро разваривают до мыльного клея. Если полученная при этом мыльная масса имеет светлый цвет и не содержит темных вкраплений, производят окончательную его отделку - частичную высолку с постановкой на ядро и подмыльный клей. Если после первого кипячения со щелочью мыло недостаточно осветлилось, то эту операцию - повторяют. [38]
Хрупкая структура металла обычно объясняется чрезмерной интенсивностью подвода тепла, вызывающей рост температуры пленки котловой воды, прилегающей к поверхности трубы, вследствие чего происходит глубокое упаривание воды. Предполагается, что высокая концентрация щелочи в упомянутой пленке разрушает защитную активную пленку на поверхности металла, что сопровождается реакцией между сталью и водой с выделением водорода. [39]
Доля аномального механизма переноса ионов ОН - увеличивается в растворах с более гидратированными катионами, например в растворах LiOH по сравнению с растворами КОН. По-видимому, при высоких концентрациях щелочи перескоки протонов происходят преимущественно через молекулы воды, входящие в гидратную оболочку катионов щелочных металлов. [40]
Доля аномального механизма переноса ионов ОН - увеличивается в растворах с более гидратированными катионами, например в растворе LiOH по сравнению с раствором КОН. По-видимому, при высоких концентрациях щелочи перескоки протонов происходят преимущественно через молекулы воды, входящие в гидратную оболочку катионов щелочных металлов. [41]
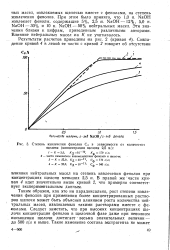 |
Степень извлечения фенолов Си в зависимости от количества щелочи ( концентрация щелочи 2 5 н.. [42] |
Таким образом, как это ни парадоксально, рост степени извлечения фенолов при применении более концентрированных растворов щелочи может быть объяснен влиянием роста количества нейтральных масел, извлекаемых такими растворами вместе с фе-юлами. Следует заметить, что при высоких концентрациях щелочи концентрация фенолов в щелочной фазе даже при неполном насыщении щелочи достигает - весьма значительных величин - до 500 г / л и выше. [43]
В отличие от золей теллура оптические характеристики золей селена сравнительно мало зависят от концентрации восстановителя. Только при очень высокой концентрации гидразина или высокой концентрации щелочи получаются частицы золя иной формы, золь обладает сероватой окраской и имеет сравнительно небольшой максимум поглощения примерно при 360 ммк. В связи с тем что гидразин заметно поглощает свет при длинах волн менее 260 ммк, желательно работать при более низких егр концентрациях и измерять оптическую плотность при 260 ммк. [44]
Исследование кинетики реакции показало, что она имеет первый порядок по катиону пиридиния и второй по гидроксил-иону. С этим согласуется наблюдение, что при высоких концентрациях щелочи лимитирующей стадией является присоединение гидроксил-иона к катиону, тогда как при более низких концентрациях ионов - ОН скорость процесса определяется стадией перехода от циклической к открытой форме. По аналогичной схеме расщепляются щелочами соли пирилия. Бензо-аналоги пирклиевого и пиридиниевого катионов дают продукты раскрытия цикла значительно труднее, и в обычных условиях в смеси преобладает циклический карбинол. [45]
Страницы: 1 2 3 4