Большая концентрация - кислота
Cтраница 3
Образованию хлористого нитрозила способствует повышение концентрации кислот в растворе. При большой концентрации кислот и высокой температуре парциальное давление паров хлористого водорода и азотной кислоты над растворами весьма велико. Это приводит к образованию больших количеств хлористого нитрозила и хлора. При применении 30 - 40 % - ной азотной кислоты и температуре до 60 - 80 С потери азота в виде хлористого нитрозила невелики. [31]
Образованию хлористого нитрозила способствует повышение концентрации кислот в растворе. При большой концентрации кислот и высокой температуре давление паров НС1 и HN03 над раствором увеличивается, что приводит к образованию больших количеств хлористого нитрозила и хлора. При охлаждении раствора из него выделяется значительная доля KN03, а маточный раствор может быть возвращен в цикл. В дальнейшем, при накоплении значительных количеств соляной кислоты, перед возвратом раствора в процесс необходимо отгонять из него часть хлористого водорода. Отгоняемые пары конденсируются в виде соляной кислоты. [32]
 |
Схема получения нитрата калия из хлористого калия и азотной кислоты. [33] |
Образованию хлористого нитрозила способствует повышение концентрации кислот в растворе. При большой концентрации кислот и высокой температуре давление паров НС1 и HNO3 над раствором увеличивается, что приводит к образованию больших количеств хлористого нитрозила и хлора. [34]
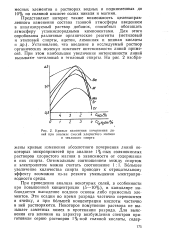
Для оксидирования алюминия и его сплавов в качестве электролита обычно применяют 15 - 20-процентный раствор серной кислоты. При большей концентрации кислоты уменьшается скорость образования пленки и увеличивается ее пористость. Большое влияние на формирование оксидного слоя окавывают температура электролита и плотность тока, при которой ведется оксидирование. С повышением температуры значительно возрастает скорость растворения окиси алюминия в кислоте. Повышение анодной плотности тока увеличивает скорость образования оксидной пленки ( фиг. Но применение чрезмерно высокой плотности тока вызывает местный перегрев электролита, а это, в свою очередь, приводит к интенсивному растворению пленки, а иногда и к растравливанию металла ( фиг. Толщина пленки увеличивается почти пропорционально количеству электричества, пропущенному через металл. Однако по достижении ею некоторой толщины начинает сказываться местный разогрев и растворимость окисла в электролите повышается, что приводит к снижению скорости наращивания пленки. [35]
Для оксидирования алюминия и его сплавов в качестве электролита обычно применяют 15 - 20-процентный раствор серной кислоты. При большей концентрации кислоты уменьшается скорость образования пленки и увеличивается ее пористость. [36]
Потери азота в виде хлористого нитрозила и хлора, удаляющихся в газовую фазу, тем больше, чем в более концентрированных растворах ведется процесс. При большой концентрации кислот в растворе и высокой температуре упругость паров хлористого водорода и азотной кислоты над раствором велика и это приводит к образованию больших количеств хлористого нитрозила и хлора, чем при малых концентрациях и низких температурах. При применении 30 - 40 % - ной азотной кислоты и при температуре до 60 - 80 потери азота в виде хлористого нитрозила невелики. [37]
Образованию хлористого нитрозила способствует повышение концентрации кислот в растворе. При большой концентрации кислот и высокой температуре давление паров НС1 и HNO3 над раствором увеличивается, что приводит к образованию больших количеств хлористого нитрозила и хлора. При охлаждении раствора из него выделяется значительная доля KNO3, а маточный раствор может быть возвращен в цикл. В дальнейшем, при накоплении значительных количеств соляной кислоты, перед возвратом раствора в процесс необходимо отгонять из него часть хлористого водорода. Отгоняемые пары конденсируются в виде соляной кислоты. [38]
Образованию хлористого нитрозила способствует повышение концентрации кислот в растворе. При большой концентрации кислот и высокой температуре давление паров НС1 и НМОз над раствором увеличивается, что приводит к образованию больших количеств хлористого нитрозила и хлора. При охлаждении раствора из него выделяется значительная доля KNOs, а маточный раствор может быть возвращен в цикл. В дальнейшем, при накоплении значительных количеств соляной кислоты, перед возвратом раствора в процесс необходимо отгонять из него часть хлористого водорода. Отгоняемые пары конденсируются в виде соляной кислоты. [39]
Например, по данным [34], кислота с концентрацией 109 % состоит на 20.5 % из орто -, на 46.2 % из пиро -, на 20.6 % из Триполи -, на 8.8 % из тетраполи -, на 3.4 % из пентаполи - и на 0.5 % из гексаполп фосфорных кислот. При больших концентрациях кислоты в ее составе появляются и превалируют только метафосфорны. [40]
Чаще всего для травления рисунков в слое SiCb применяют разбавленную плавиковую кислоту. При больших концентрациях кислоты скорость травления увеличивается, при малых рН граница поли-меризованной пленки фоторезиста получается размытой. [41]
Это можно было бы объяснить тем, что уравнение Смолуховского неприменимо для диафрагм из проводника, каким является карбид титана. Действительно, при больших концентрациях кислоты или щелочи поверхность диэлектрик / раствор заменяется на поверхность проводник / раствор. Однако аналогичные эффекты обнаружены нами и при использовании индиферент-ного электролита ( КО), а также на кварцевых диафрагмах с теми же электролитами. Здесь уже не может быть принципиальных возражений против применения уравнения Смолуховского. [42]
Удобным методом концентрирования является экстракция ТБФ из нитратной среды, которая упоминалась выше. При работе с роданидом следует избегать больших концентраций кислоты и сильных окислителей. [43]
В тех случаях, когда преобладающим процессом оказывается вытеснение, отмечается лишь более пологий ход кривой при больших концентрациях кислоты; это характерно для малогидратпрованных ионов, например, ионов цезия или радия. В тех же случаях, когда преобладающим процессом при больших концентрациях кислоты оказывается дегидратация, на кривой зависимости поглощения от концентрации кислоты наблюдается минимум; такое явление характерно для сильногидратированных ионов, например, ионов лития и кальция. [44]
 |
Кривые изменения почернения линий при анализе смесей хлористого магния и этилового спирта. [45] |
Страницы: 1 2 3 4