Большая концентрация - щелочь
Cтраница 1
Большие концентрации щелочи в котловой воде образуются в заклепочных и вальцовочных соединениях в местах неплотностей. При испарении котловой воды в зазоре повышается концентрация содержащихся в ней солей, в том числе едкого натра. [1]
Большая концентрация щелочи, перегревы, содействуют такой нежелательной реакции. [2]
При большой концентрации щелочи и малом количестве восстановителя образуются ионы манганата согласно уравнению. [3]
При большой концентрации щелочи или большом зарядном токе образуется Y-NiOOH с большим удельным объемом, что приводит к набуханию электрода. [4]
 |
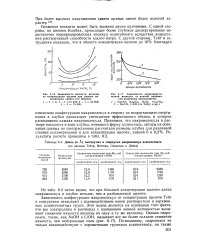
Влияние рН на скорость коррозии железа в воде. [5] |
При большой концентрации щелочи и повышенной температуре скорость коррозии железа увеличивается. Процесс протекает с образованием анионов гипоферри-та FeO - и выделением водорода. [6]
При большой концентрации щелочи или большом зарядном токе образуется у - МКЮН с большим удельным объемом, что приводит к набуханию электрода. [7]
При больших концентрациях щелочи ферриты более устойчивы и, переходя в силу диффузии к положительной пластине, отравляют ее активную массу. [8]
Это объясняется тем, что при большой концентрации щелочи возрастает гигроскопичность моющих препаратов. При сушке на поверхности обезжиренных деталей может образовываться налет карбонатов, а такие металлы, как цинк, алюминий и их сплавы, могут подвергаться травлению. [9]
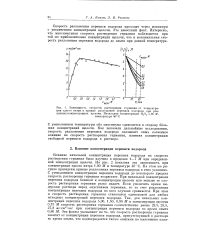 |
Зависимость скорости растворения германия от концентрации едкого натра и кривые разложения перекиси водорода при различных концентрациях щелочи. Начальная концентрация Н20о 5 80 М. [10] |
С уменьшением температуры оба максимума сдвигаются в сторону больших концентраций щелочи. Как показали дальнейшие исследования, скорость разложения перекиси водорода оказывает лишь косвенное влияние на скорость растворения германия, изменяя концентрацию свободной перекиси водорода в растворе. [11]
Из табл. 8.2 четко видно, что при большей концентрации щелочи длина макромолекул в клубке меньше, чем в разбавленной щелочи. [13]
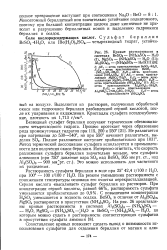 |
Кривые растворимости в системах BeSO4 - ( NH4 2SO4 - Н2О ( I, MgSO4 - ( NH4 2SO4 - Н2О ( II. A12 ( S04 3 - ( NH4 2S04 - H2O ( III. [14] |
Моноатомный бериллатный ион значительно устойчивее полиатомного, поэтому при большой концентрации щелочи даже кипячение не приводит к разрушению бериллатных ионов и выделению гидроокиси бериллия в осадок. [15]
Страницы: 1 2 3 4