Большая концентрация - щелочь
Cтраница 3
Качзство оксидных пленок значительно ухудшается в случае нарушения состава раствора и режима работы. При чрезмерно большой концентрации щелочи или высокой температуре образуются рыхлые пленки. Значительное увеличение продолжительности оксидирования может привести к растравливанию металла. При малой концентрации в растворе щелочи или при низкой температуре образуются тонкие пленки, имеющие цвета побежалости. [31]
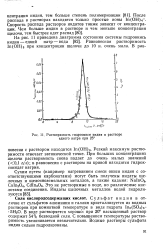 |
Растворимость гидроокиси индия в растворе едкого натра при 25. [32] |
Резкий максимум растворимости отвечает эвтонической точке. При больших концентрациях щелочи растворимость снова падает до очень малых значений ( 0 1 г / л); в равновесии с раствором на кривой находится гидрок-соиндат натрия. [33]
Отработанные щелочи интенсивно поглощают кислород. При больших концентрациях щелочей вода в водоеме может на большом протяжении терять растворенный кислород. [34]
Качество получаемой оксидной пленки значительно ухудшается при нарушении состава ванны и режима работы. Так, при чрезмерно большой концентрации щелочи или высокой температуре образуются рыхлые пленки. Значительное увеличение продолжительности оксидирования может привести к растравливанию поверхности металла. При малой концентрации едкого натра или низкой температуре образуются тонкие пленки, имеющие цвета побежалости. После оксидирования детали промывают в холодной, а затем в теплой воде и просушивают в термостате или сжатым воздухом. Пассивирование производится при температуре 15 - 25 погружением деталей на 2 - 10 сек. При этом происходит нейтрализация остатков щелочи и пассивирование металла в порах пленки, что приводит к повышению стойкости деталей против коррозии. Обработка пленки при - - более высоких температурах приводит к ухудшению качества, а иногда и к разрушению пленки. [35]
Для аналитических целей определение Сг в виде CrOii лучше проводить на фоне едких щелочей; получается одна хорошо выраженная волна хромат-иона [ Ei / - 0 85 в ( нас. NaOH ( КОН); при большей концентрации щелочи диффузной - ный ток хрома уменьшается. [36]
Для выбора оптимальной концентрации щелочи необходимо знать зависимость удельной электропроводности растворов от концентрации при различных температурах. С повышением температуры максимумы сдвигаются в сторону больших концентраций щелочи. [37]
Скорость реакции Канниццаро - Тищенко и соотношение количеств продуктов, получаемых по упомянутой реакции и реакции альдольного уплотнения, зависят от условий ведения процесса. Например, найдено [12, 13], что при больших концентрациях щелочи идет, главным образом, реакция Канниццаро. [38]
Чему равен порядок этой реакции: а) при малой, б) при большой концентрации щелочи. [39]
Меервейна-Пондорфа такой ион не образуется и гидридный иоь мог бы перемешаться только под влиянием притяжения со стороны положительно зараженного центра. В условиях реакции Канниццаро взаимодействие гидридных ионов с протонами из воды может быть затруднено из-за большой концентрации щелочи, поэтому возможность перемещения ионов Н - к положительному углероду карбонильной группы альдегида не полностью исключена. В условиях же реакции Меервейна - Пондорфа последняя возможность исключается, так как в реакционной смеси имеются сильные алкоксикислоты HA1 ( OR) 4 [527], протоны которых будут реагировать с ионами Н в первую очередь, давая молекулярный водород. Их правильность видна еще и из того, что восстановление альдегидов гидридами металлов никогда не проводят в кислых растворах [834], а также из того, что восстановление гидридами ненасыщенных альдегидов приводит к гидрированию не только альдегидной группы, но и двойной связи [643], чего никогда не бывает при реакции Меервейна-Пондорфа. [40]
Из работ [21, 52, 103, 104, 171, 177, 178] следует, что при гидрировании карбонильных соединений щелочь оказывает активирующее влияние на катализатор. NaOH, причем с изменением температуры от 0 до 60 максимум скорости реакции сдвигается в сторону больших концентраций щелочи. [41]
 |
Кинетические и потенциальные кривые гидрирования орто-нитрофенола на платиновом катализаторе в зависимости от концентрации щелочи в. [42] |
Увеличение концентрации щелочи в растворе неблагоприятно сказывается на активации водорода, что приводит к изменению стадии, лимитирующей реакцию. Увеличение энергии связи водорода с поверхностью при этом уменьшает скорость притока водорода из газовой фазы, особенно при больших концентрациях щелочи, следствием чего является извлечение из катализатора водорода орто-нитрофенолрм наряду с идущим гидрированием орто-нитрофенола водородом газовой фазы. Таким образом, полученные кривые представляют интегральный результат гидрирования вещества и насыщения катализатора. Поэтому максимумы и минимумы на кинетических кривых, полученные при восстановлении орто-нитрофенола, не отражают селективность процесса восстановления нитрогруппы. [43]
 |
Коэффициенты распределения гидропероксидов между оксидатом и водным раствором NaOH [ 177, 182. [44] |
В табл. 2.14 приведены коэффициенты распределения гидропероксидов между оксидатом и раствором NaOH различной концентрации. При обработке смеси гидропероксидов растворами щелочи с концентрацией 4 - 8 % в щелочной раствор переходят ди - и оксигидропероксиды в виде натриевых солей. При большей концентрации щелочи извлекается частично также и моногидропероксид. [45]
Страницы: 1 2 3 4