Аналитическая концентрация
Cтраница 2
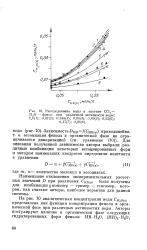 |
Распределение воды в системе СС14 - И20 - фенол при различной активности воды. [16] |
На рис. 10 аналитическая концентрация воды Сц2о ( о) представлена как функция концентрации фенола в органической фазе при различных активностях воды. [17]
В гомогенной среде аналитические концентрации реагентов относительно легко измеримы и достаточно просто связаны с концентрациями реакционноспособных частиц, скорость превращения которых определяет кинетику всего процесса. Иначе обстоит дело в гетерогенном катализе, где концентрации в жидкой и газообразной фазах связаны с концентрациями адсорбированных частиц законами равновесия, в которых роль твердого вещества до сих пор не выяснена. Хотя механизм процессов в адсорбированной фазе не установлен, формальную кинетику процесса можно определить в том случае, если площадь поверхности катализатора и его природа не изменяются. [18]
Квадратные скобки обозначают аналитическую концентрацию ( моляр-ность, моляльность) ионов А и В; а и Ь - абсолютные заряды ионов А и В соответственно. [19]
В растворе с аналитической концентрацией с концентрация мономерных ионов равна саг, где а. Концентрация димеров уменьшается за счет образования простых ионов и ионных тройников. Степень диссоциации аа умножена на три, так как на образование двух ионных тройников тратится три ионные пары. [20]
В растворе с аналитической концентрацией с концентрация мономерных ионов равна са, где ai - степень диссоциации вещества на мономерные ионы; концентрация ионных тройников соответственно равна а3с, где а3 - степень диссоциации на ионные тройники; концентрация недиссощиированных молекул - ионных пар, соответственно равна с ( 1 - cii - За3); концентрация димеров уменьшается за счет образования простых конов и ионных тройников. Степень диссоциации сс3 умножена на три, так как на образование двух ионных тройников тратится три ионные пары. [21]
В это уоавнение входят аналитические концентрации или же массы обменивающихся ионов в твердой и жидкой фазах. [22]
 |
Кривые образования для систем. [23] |
С и Ct - аналитические концентрации кадмия и хлора, даваемые уравнением материального баланса ( 25) через концентрации индивидуальных комплексов. [24]
Квадратные скобки [ ] обозначают аналитические концентрации индивидуальных компонентов. [25]
При расчетах рН использование аналитических концентраций допустимо для разбавленных растворов, в которых активности ионов равны их концентрациям. [26]
При расчетах рН использование аналитических концентраций допустимо только для очень разбавленных растворов, в которых активности практически равны концентрациям ионов. Покажем, как влияет на расчетное значение рН переход к активности ионов водорода. [27]
Она не зависит от аналитических концентраций Me и Y, но зависит от рН и концентрации присутствующего буферного вещества. [28]
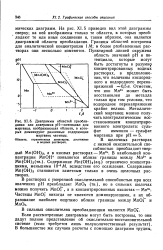 |
Диаграммы областей преобладания или диаграмма рН - потенциал для марганца, изображающая области, в которых доминируют различные содержащие марганец частицы. [29] |
Границы областей построены для аналитической концентрации I M; в более разбавленных растворах они несколько изменятся. [30]
Страницы: 1 2 3 4