Равновесная концентрация - ион - водород
Cтраница 1
Равновесные концентрации ионов водорода и анионов кислот средней силы вследствие неполной диссоциации электролита до начала титрования меньше концентрации исходной кислоты, но все же отличаются достаточно высокими значениями и заметно влияют на электропроводность раствора. С уменьшением силы кислоты концентрации Н - и АП - - ИОНОВ все более понижаются и при значении р / Са 5 они уже практически перестают оказывать влияние на электропроводность раствора. При титровании концентрация ионов водорода нелинейно понижается, а анионов кислоты нелинейно увеличивается и в точке эквивалентности достигает максимальной величины, равной концентрации кислоты. [1]
 |
Зависимость выходов для системы одноядерных комплексов от lg [ L ]. [2] |
Увеличение равновесной концентрации ионов водорода [ Н ] в системе усиливает протонизацию лиганда-аниона слабой кислоты, уменьшает его равновесную концентрацию и приводит к смещению на диаграмме a; - IglL ] по абсциссе влево вплоть до полного разрушения комплексов. [3]
Данные для малых равновесных концентраций ионов водорода при экстракции дибутиловым эфиром отсутствуют, так как получение их затруднено очень малой экстрагирующей способностью дибутилового эфира в этих условиях. [4]
Для более слабых кислот равновесные концентрации ионов водорода настолько малы, что они практически не могут оказывать влияние на электропроводность раствора в продолжение всего процесса титрования. [5]
Это говорит о постоянстве Кп в широком интервале равновесных концентраций ионов водорода, натрия и аминокислоты. В этих условиях аминокислота находится в фазе ионита как в виде катиона, так и в виде цвиттер-иона. [6]
Очевидно, что, зная х, легко вычислить равновесную концентрацию ионов водорода. Уравнение (19.10) может быть точно решено относительно Н как квадратное уравнение в предположении, что х известно. Но является ли этот путь наиболее простым. [7]
Таким образом, в процессе титрования сильной кислоты сильным основанием равновесная концентрация ионов водорода складывается из ионов водорода сильной кислоты и ионов воцороца, образующихся при диссоциации воды. Концентрация последних ничтожно мала, и если раствор сильной кислоты не очень разбавлен, ею можно пренебречь. [8]
В соотношениях (5.4), ( 5.4), (5.6) фигурируют равновесные концентрации ионов водорода и гидроксильных групп. [9]
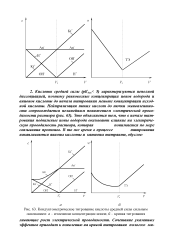 |
Кондуктометрическое титрование кислоты средней силы сильным основанием. а - изменение концентрации ионов. 6 - кривая титрования. [10] |
Кислоты средней силы ( рКдис 5) характеризуются неполной диссоциацией, поэтому равновесные концентрации ионов водорода и анионов кислоты до начала титрования меньше концентрации исходной кислоты. Это объясняется тем, что в начале титрования подвижные ионы водорода оказывают влияние на электрическую проводимость раствора, которая понижается по мере связывания протонов. [11]
Вызывает тревогу возможная низкая точность определения входящей в эти формулы разности между равновесной концентрацией ионов водорода и концентрацией добавки сильной кислоты. [12]
Поскольку [ H J - величина большая и практически постоянная, коэффициент распределения определяется только равновесной концентрацией ионов водорода в органической фазе. Если галогеноводородная кислота НХ плохо экстрагируется и ( или) слабо диссоциирует в экстракте, не влияя на величину [ Н ] 0, то D зависит от присутствия макроэлемента. В самом деле, когда макрокомпонент экстрагируется и его комплексная кислота, будучи очень сильной кислотой, существенно увеличивает величину [ Н ] 0, коэффициент распределения микроэлемента должен уменьшаться. [13]
В основе определения / Сд и а уксусной кислоты ( слабого электролита) лежит измерение равновесной концентрации ионов водорода [ Н ] раствора известной концентрации. [14]
В отличие от рН значение р [ Н ] связано не с активностью, а с равновесной концентрацией ионов водорода. Оно должно быть либо измерено на соответствующим образом калиброванном рН - метре, либо пересчитано из значения рН путем внесения поправок на коэффициент активности. [15]
Страницы: 1 2