Равновесная концентрация - кислород
Cтраница 1
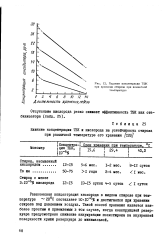 |
Падение концентрации ТБК при хранении стирола при комнатной температуре. [1] |
Равновесная концентрация кислорода в жидком стироле при температуре - 20 С составляет 50 - 10 - у я достигается прж хранении стирола под давлением воздуха. Такой способ хранения является наиболее простым и приемлемым в том случае, когда конструкцией резервуара предусмотрено снижение аккумуляции полистирола на внутренней поверхности крыши резервуара до минимальной. [2]
 |
Максимальная растворимость кислорода в jj железе и равновесная концентрация кислорода при наличии в расплаве Si и С при различных температурах. [3] |
Равновесные концентрации кислорода при наличии в расплавленном железе различных концентраций раскислителей могут быть рассчитаны на основании известных температурных зависимостей констант равновесия различных реакций. [4]
Сг - равновесная концентрация кислорода, взятая из табл. 2 для температуры воды, измеренной при отборе пробы, с возможной поправкой на атмосферное давление и на содержание растворенных солей. Результаты округляются до 0 1 мг или до целых процентов. [5]
При температурах 1300 С равновесная концентрация кислорода значительно ниже содержания кислорода в газе-теплоносителе. При этой температуре реакция окисления затормаживается. Как правило, обжиг окатышей из магнетитовых концентратов ведут в интервале температур 1250 - 1300 С, что исключает диссоциацию гематита. В процессе нагрева стремятся к максимальному окислению магнетита. Своевременное завершение процесса окисления, активность свежеполученного гематита обусловливают рост скорости спекания частиц, получение малопористой плотной структуры, отсутствие двухзонной гематито-магнетитовой структуры и напряжений в окатышах. [6]
С ростом температуры увеличивается равновесная концентрация кислорода, что вызывает уменьшение раскислительной способности растворенных веществ. [7]
В практике аэрации сточных вод равновесные концентрации кислорода в жидкости никогда не достигаются. Действительные или рабочие концентрации кислорода С в жидкости всегда отличаются от равновесных С Разность между этими концентрациями, характеризующая степень отклонения от равновесия, и представляет собой движущую силу диффузионного процесса. Примем следующие основные допущения; 1) движение газовых пузырьков сферической формы через слой жидкости происходит в режиме Стокса; 2) концевые эффекты растворения кислорода, обусловленные ускорением массопередачи в моменты образования воздушных пузырьков и выхлопа на поверхность, отсутствуют; 3) процесс конвективной диффузии кислорода квазистационарен. [8]
С в уравнении (6.5) - это равновесная концентрация кислорода, соответствующая по закону Генри [ уравнение (6.6) ] парциальному давлению кислорода в газовой фазе рг. [9]
Для каждого раскислителя раскис-лительная способность характеризуется равновесной концентрацией кислорода при постоянной температуре. [10]
Для каждого раскнслителя раскис-лительная способность характеризуется равновесной концентрацией кислорода при постоянной температуре. [11]
Для каждого раскислителя раскис-лительная способность характеризуется равновесной концентрацией кислорода при постоянной температуре. [12]
Повышение концентрации S02 в исходном газе приводит к более низкой равновесной концентрации кислорода и к уменьшению равновесного превращения S02 в S03 при данных температурах. Таким образом, промышленные катализаторы должны быть активными в диапазоне температур 400 - 500 С. [13]
 |
Растворимость кислорода в различных жидкостях при 37 С. [14] |
В табл. 4.4 приведены коэффициенты распределения, а также равновесные концентрации кислорода при 37 С, которые определены экспериментально для глюкозо-солевых растворов и полусинтетической питательной среды ПС, содержащей в своем составе аминокислоты и сыворотку крупного рогатого скота. [15]
Страницы: 1 2 3