Равновесная концентрация - кислород
Cтраница 3
Как уже было указано, для упрощения вычислений эквивалентный диаметр пузырька и скорость его подъема приняты постоянными и соответствующими их значениям при h Н / 2; изменением объема вследствие убыли кислорода пренебрегаем. Погрешность допущения о постоянстве величины Ст - равновесной концентрации кислорода - целесообразно оценить, так как она возрастает по мере возрастания степени использования кислорода А. [31]
Элементы-раскислители действуют на скорость десульфурации чугуна, по-видимому, за счет изменения как термодинамических, так и кинетических условий. Изменяется коэффициент активности серы в чугуне и уменьшается равновесная концентрация кислорода. Снижение концентрации кислорода в шлаке вызывает увеличение коэффициента распределения серы между шлаком и металлом. Рокка, Грант и Чипман [24] показали это экспериментально в случае распределения серы между чистым железом н шлаками доменного типа. [32]
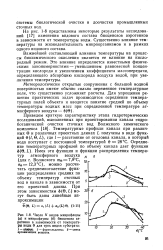 |
Число N видов микрофлоры ( а и микрофауны ( б биоценоза аэ-ротенка в зависимости от температуры воды Ф для трех видов субстрата. [33] |
Важнейшей составляющей влияния температуры на процессы биохимического окисления является ее влияние на кислородный режим. Это влияние определяется известными физическими закономерностями - уменьшением равновесной концентрации кислорода и увеличением коэффициента массопередачи, определяющего абсорбцию кислорода воздуха водой, при увеличении температуры. [34]
 |
Окисление сульфидов и других соединений кислородом в водных растворах. [35] |
В табл. 37 приведены расчеты возможности окисления некоторых простых сульфидов кислородом в пульпе. Все рассмотренные здесь реакции имеют высокие константы равновесия, что указывает на их направленность и малую равновесную концентрацию кислорода в растворе, но, конечно, ничего не говорит о скорости. Часть кислорода расходуется на окисление цианида, переходящего при этом в бесполезный для передела цианат, а сера связывает цианид в роданид. [36]
Эффективность процесса очистки от кислорода растворами V2 зависит, конечно, как от равновесной концентрации кислорода в присутствии У2 - ионов, так и от скорости поглощения кислорода этим реактивом. Однако можно с уверенностью сказать, что в присутствии большого избытка такого сильного восстановителя, как двухвалентный ванадий, равновесная концентрация кислорода будет ничтожно мала. Кроме того, наблюдаемое во время опыта изменение цвета раствора указывает на то, что поглощение кислорода происходит мгновенно. [37]
Вывод о том, что при высоких температурах процесс взаимодействия углерода с СО определяется равновесной концентрацией кислорода, вполне естествен, так как условие a - К. Что же касается второго вывода о том, что при достаточно низких температурах ( кинетический режим для реакции С О2) процесс взаимодействия углерода с СО2 в основном определяется равновесной концентрацией кислорода, то он является в некоторой степени неожиданным. [38]
При этом получались газообразный азот и обогащенная кислородом жидкость, которая дросселировалась в межтрубное пространство трубчатки в качестве хладоагента. Если учесть, что равновесная концентрация кислорода в жидкости равна 55 %, мтэжно сделать вывод о недостаточности четкости разделения в опытной трубчатке Клода. [39]
Восстановительные группы могут перескакивать в матрице полимера из одного фиксированного положения в другое. К такому типу редокситов можно отнести обычные полимеризационные или поликонденсац онные ио-ниты, насыщенные ионами переменной валентности. Имея в виду, что равновесная концентрация кислорода в воде ограничена его растворимостью и на два-три порядка меньше концентрации восстановительных групп, вполне реален такой случай, когда общий поток восстановительных групп к поверхности зерна в фазе редоксита будет больше соответствующего потока кислорода. [40]
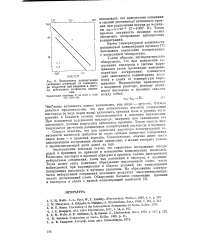 |
Зависимость концентрации телей в слоях от температуры выра-свободных носителей от температу - ЩИВания. Выращивание производится. [41] |
Отсюда делается предположение, что при относительно высоком содержании кислорода ( в виде паров воды) активность кремния мала и уровень легирования в большей степени обусловливается в основном кислородом. При понижении содержания кислорода, например при связывании его алюминием, должна возрастать активность кремния. Такая модель подтверждается расчетами равновесных концентраций кислорода и кремния. [42]
Необходимым условием определения окислительного потенциала колориметрическим методом является быстрое установление равновесия между индикатором и исследуемой системой. Поэтому в системах, в которых процессы окисления-восстановления осуществляются с участием водорода или кислорода, измерение окислительных потенциалов следует производить в присутствии катализаторов, ускоряющих окислительно-восстановительную реакцию. Кроме того, необходимо, чтобы при измерениях потенциала систем типа ( II), в которых процесс восстановления осуществляется водородом, окисленная форма индикатора достаточно быстро восстанавливалась. Аналогично для окислительно-восстановительных систем типа ( III) измерения потенциала в принципе возможны только в случае, если восстановленная форма индикатора быстро окисляется кислородом. Это требует, в свою очередь, тщательного удаления примесного кислорода, концентрация которого должна быть меньше, чем равновесная концентрация кислорода, выделяемого в течение окислительно-восстановительной реакции. [43]
Страницы: 1 2 3