Равновесная концентрация - окись - азот
Cтраница 2
 |
Затраты электроэнергии на получение 1 т NO. [16] |
Глика и др. [4] и могут быть положены в основу расчета плазмоструйного реактора. Нас интересует время установления равновесной концентрации окиси азота и объем реактора. В работе Ю. П. Райзера [5] приведены данные о времени установления равновесия в условиях взрыва в воздухе, но в форме, неудобной для расчета плазмоструйного реактора. Нами проведен более полный расчет. [17]
Расчет был произведен для стехиометрической азотно-кислород-ной смеси, изотермических условий и давления 1 апга. Как следует из графика, равновесная концентрация окиси азота, равная примерно 7 8 %, достигалась за время около 2 - 1СГ4 сек. [19]
В первом приближении можно считать, что температура сперва мгновенно возрастает, достигая максимального значения, а затем плавно падает. По мере падения температуры уменьшается и равновесная концентрация окиси азота. NO ] 00, ( N0) 0 0 и, следовательно, идет образование окиси азота. [20]
Результаты расчетов представлены на рис. 5, где равновесная концентрация окиси азота дана в процентах к исходной смеси и равна концентрации окиси азота в охлажденной смеси при идеальной закалке. [21]
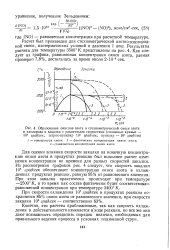
Как видно из рис. 1 - 1, кривая равновесного содержания окиси азота имеет максимум, абсолютное значение которого относительно оси температур очень сильно зависит от давления. С повышением давления, что следует также из принципа Ле-Шателье, равновесная концентрация окиси азота увеличивается, а значения оптимальных температур смещаются в сторону более высоких. [22]
Если процесс проводить в пределах температур, при которых не происходит диссоциации N2 и О2 на атомы, давление не влияет на равновесие реакции. При проведении синтеза окиси азота в области высоких температур в расчетах равновесной концентрации окиси азота необходимо учитывать диссоциацию N2 и О2 на атомы. [23]
Данная классификация, на наш взгляд, неудачна, а примеры, иллюстрирующие различные типы реакций, недостаточно убедительны. Так, получение окиси азота следует отнести к реакциям первого типа, поскольку равновесная концентрация окиси азота максимальна при высоких температурах. [24]
Как уже говорилось в § 1 настоящей главы, разложение окиси азота - экзотермический процесс, и равновесная концентрация окиси азота падает с уменьшением температуры. [25]
В таком виде закон действующих масс не учитывает диссоциации молекул на атомы, вполне реальной при температурах, для которых равновесная концентрация окиси азота становится заметной. Таким образом, предельные стационарные концентрации окиси азота, полученные в наших опытах при пониженных давлениях, заметно выше максимально возможной равновесной концентрации для атмосферного давления и значительно выше максимальных равновесных концентраций при равных давлениях. [26]
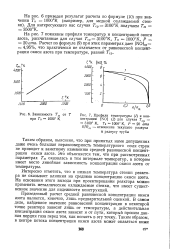 |
Профили температуры ( / и концентрации [ NO ] ( 2 для случая Г 3100 К, Го 1000 К, Р 20 ста RlRm - отношение текущего радиуса к радиусу трубы. [27] |
На рис. 7 показаны профили температур и концентраций окиси азота, рассчитанные для случая 7ср3100оК, Т0 1000 К, Р 20 arm. Расчет по формуле ( 9) при этих параметрах дает [ NO ] cp 4 95 %, что практически не отличается от равновесной концентрации окиси азота при температуре, равной Гер. [28]
Если, например, известны давление Р и коэффициент избытка воздуха ав, то можно подобрать соответствующий график, на котором находят точки пересечения линии постоянной температуры воздуха U при заданной температуре топлива Ь с линией добавки кислорода АО2 и определяют остальные параметры процесса: энтальпию, температуру в реакторе и равновесную концентрацию окиси азота. [29]
Если, например, известны давление Р и коэффициент избытка воздуха ав, то можно подобрать соответствующий график, на котором находят точки пересечения линии постоянной температуры воздуха / в при заданной температуре топлива / т с линией добавки кислорода АО2 и определяют остальные параметры процесса: энтальпию, температуру в реакторе и равновесную концентрацию окиси азота. [30]
Страницы: 1 2 3